Que conclure des nouveaux essais sur les inhibiteurs de PARP et les sur la chirurgie ?
De nombreux essais ont été publiés ces derniers mois dans la prise en charge des cancers de l’ovaire, en particulier sur l’efficacité des inhibiteurs de PARP et sur la place de la chirurgie. De manière pragmatique, le Pr Fabrice Lécuru et le Dr Frédéric Selle font le point sur ce qu’il faut retenir de ces études et quelles en sont les implications en pratique.
Le regard du chirurgien
Dr Frédéric Selle : Quelles sont les modalités en 2021 de la prise en charge chirurgicale des cancers de l’ovaire de stades limités et notamment la place des curages, dans la re-stadification ou d’emblée ?
Pr Fabrice Lécuru : Il n’y a pas eu de grandes nouveautés sur la chirurgie des stades précoces. Je rappelle que cette chirurgie répond à deux objectifs distincts. Le premier est l’exérèse de la ou des masses ovariennes, de préférence sans rupture, puisqu’aux stades précoces, logiquement, il n’y a pas de maladie visible en dehors des annexes. La voie d’abord, cœlioscopie ou laparotomie, sera choisie en fonction de son expérience et de la taille de la ou des masses de façon à pouvoir les enlever sans les rompre. Le second objectif de cette chirurgie est la stadification, qui reste péritonéale ou omentale et ganglionnaire. Dans les recommandations ESGO, je trouve que la formulation est un peu floue : il est dit que les curages sont réalisés dans les situations où cela va changer le traitement adjuvant. Ainsi, dans les cancers séreux de haut grade, le curage n’est théoriquement pas nécessaire puisque de toute façon il y aura une indication de chimiothérapie. Cependant, un stade IIIA, donc avec atteinte ganglionnaire, pourrait être une indication aux inhibiteurs de PARP (25 à 30 % des patientes “macroscopiquement” stade I-II). Dans ces conditions, il faut proposer un curage de stadification aux patients potentiellement éligibles à un inhibiteur de PARP d’après leur histologie. Bien sûr, ces aspects ne concernent que les patientes dont le bilan d’imagerie est normal. Il est évident qu’en cas d’adénopathies visibles sur le scanner préopératoire, le curage est nécessaire.
Le type histologique joue donc également un rôle sur l’indication du curage en dehors des séreux de haut grade.
Il y a par ailleurs quelques particularités. Pour les cancers endométrioïdes de bas grade, le curage n’est pas nécessaire, car cela ne changera pas la prise en charge ultérieure (à condition d’avoir une imagerie normale). De plus, ces patientes sont à très faible risque d’extension ganglionnaire. C’est également le cas pour les cancers mucineux expansifs. Concernant les cancers à cellules claires, qui sont très lymphophiles et peu chimiosensibles, la tendance est de proposer des curages de façon systématique.
Le type histologique joue donc également un rôle sur l’indication du curage en dehors des séreux de haut grade.
Dr Frédéric Selle : Que faire quand le type histologique n’est pas clairement défini ?
Pr Fabrice Lécuru : On raisonne toujours sur un type histologique bien précis et parfaitement connu mais, dans certaines situations, le diagnostic n’est pas évident en peropératoire (par exemple nous pouvons parfois hésiter entre une tumeur mucineuse frontière et un cancer mucineux limité à un ovaire). Ainsi, dans certains cas, notamment pour les tumeurs rares, il y aura un bénéfice à faire la chirurgie en deux temps : d’abord un temps diagnostique, puis un temps de stadification. Cependant, il faut savoir que cela pose des problèmes techniques en chirurgie et que cela majore le risque périopératoire. En effet, les patientes sont reprises 3 semaines à 1 mois après la première intervention, en pleine période d’inflammation au niveau du péritoine, et du rétropéritoine. Les dissections ganglionnaires sont alors moins faciles qu’en situation de chirurgie première. Ainsi, quand il est possible d’avoir un examen extemporané, il est préférable de faire la totalité du geste dans le même temps opératoire. Ces “petites” subtilités me semblent importantes.
Dr Frédéric Selle : Quelles sont les conséquences en pratique courante des résultats de l’étude LION évaluant la place des curages ganglionnaires en chirurgie initiale dans les cancers de l’ovaire de stades avancés ?
Pr Fabrice Lécuru : Cette étude est à beaucoup d’égards une référence dans les validations de stratégies chirurgicales. Il faut rappeler qu’avant cet essai à peu près toutes les études rétrospectives, les études sur les bases de données, notamment la SEER, les études rétrospectives des bases prospectives des essais AGO et GINECO avaient montré le bénéfice en termes de survie de la réalisation des curages lors des chirurgies des stades avancés, en particulier quand la chirurgie était complète. L’essai thérapeutique LION, qui est une étude bien réalisée, a montré l’inverse : chez les malades qui n’ont pas d’adénopathies, il n’y a pas de bénéfice en survie globale à réaliser un curage par rapport à laisser les ganglions en place alors même (l’étude le montre) que des ganglions malades microscopiquement subsistent dans environ 45 % des cas. Ainsi, aujourd’hui, il est recommandé de ne plus faire de curage systématique chez les patientes qui sont en résection complète et qui n’ont pas d’adénopathies ni visibles à l’imagerie, ni à l’exploration chirurgicale. Il faudrait théoriquement disséquer le péritoine pour vérifier l’absence de ganglions visibles. À noter tout de même qu’il s’agit d’un essai AGO, c’est-à-dire allemand, dans lequel les patientes sont très majoritairement opérées en chirurgie première. En France, la situation est un peu différente puisque 60 % des patientes ont une chimiothérapie néoadjuvante et une chirurgie d’intervalle. La question se posait donc de l’extrapolation des résultats de LION dans ces cas. Bien que n’ayant pas de données très solides en la matière, s’il n’y pas de ganglions au départ et qu’il n’y en a toujours pas au moment de la chirurgie d’intervalle, je pense que l’on se retrouve dans la situation de l’essai et on pourra donc omettre les curages. S’il y a des ganglions au départ et qu’il en persiste au moment de la chirurgie d’intervalle alors la décision est simple : curages. La question va se poser pour les cas où il y a des ganglions au départ et qu’il n’y en a plus au moment de la chirurgie d’intervalle. Pour cette situation, nous n’avons pas de données. La prudence serait de continuer à faire des curages pour ces patientes. J’attends avec impatience que Jean-Marc Classe publie les résultats de CARACO dans lequel il y a ce type de population. Je rappelle que l’un des résultats majeurs de LION avait été de montrer la morbi-mortalité des curages, donc il n’y a vraiment plus aucune indication à les faire systématiquement pour les patientes qui répondent aux critères de l’étude LION.
Dr Frédéric Selle : Pour les patientes qui ont des adénopathies initiales, mais qui n’ont plus de ganglions visibles, les recommandations de Saint-Paul-de-Vence préconisent de discuter au cas par cas alors que tu suggères le curage. Pourrais-tu préciser ?
Pr Fabrice Lécuru : Généralement, quand il est conseillé le cas par cas, c’est qu’on ne sait pas vraiment ce qu’il faut faire par manque de données notamment… Alors bien sûr, dans cette situation, nous allons discuter en fonction du cas. Cependant, en dehors des centres experts, ma recommandation serait de faire tout de même des curages.
Dr Frédéric Selle : Concernant la chirurgie de la première rechute platine sensible des cancers de l’ovaire, plusieurs essais paraissent contradictoires. Comment analyses-tu ces résultats ?
Pr Fabrice Lécuru : Nous nous trouvons ici aussi dans un cas d’école. Après la qualité de l’étude LION, nous avons de nouveau la démonstration de ce que peut générer un essai particulièrement bien réalisé par rapport à un essai qui comporte quelques limites méthodologiques. L’essai américain est souvent présenté comme concluant que la chirurgie donne de moins bons résultats que le traitement médical, alors que ce n’est pas ce qui est montré : il n’y a pas de différence significative. L’essai allemand est positif en survie sans progression et en survie globale et l’essai chinois positif en survie sans progression pour le moment. Ce qui différencie principalement l’essai américain des deux autres est le mode de sélection des patientes. Dans l’essai chinois et dans l’essai allemand, il y a un score objectif qui est utilisé pour décider à qui l’opération sera proposée ou non. Dans l’essai américain, c’est l’avis d’un praticien qui est utilisé pour cette décision. La deuxième grande différence est le taux de résection complète, c’est-à-dire la qualité de la chirurgie qui est bien meilleure pour l’essai chinois et l’essai allemand, alors qu’elle est faible dans l’essai américain. On connaît tous l’importance de la résection complète pour le pronostic des patientes. Le troisième paramètre à prendre en compte est l’utilisation du bévacizumab dans l’essai américain alors qu’il était très minoritaire dans les deux autres. En fait, cet essai américain était un mix entre une question sur l’effet de la chirurgie et une autre sur l’intérêt du bévacizumab en situation de rechute platine sensible. Voilà donc une explication des résultats en apparence divergents entre les essais. J’ajouterai que les résultats connus de l’essai américain sont issus d’une analyse intermédiaire comprenant la moitié des effectifs nécessaires, avec des intervalles de confiance extrêmement larges, ce qui n’est pas le cas des autres essais qui sont allés au bout des inclusions prévues initialement.
On connaît tous l’importance de la résection complète pour le pronostic des patientes.
Dr Frédéric Selle : Que peut-on en conclure en pratique et quelles sont les nouvelles recommandations en situation de rechute platine sensible ?
Ce que montrent ces études, en particulier les essais chinois et allemand, c’est que la chirurgie, chez des patientes sélectionnées, quand celle-ci est bien réalisée, avec un taux de résection complète important, procure un bénéfice en termes de survie, et que les malades qui en bénéficient le plus sont celles qui sont en résection complète. Inversement, les patientes qui ne sont pas en résection complète ont des courbes de survie qui sont inférieures à celles du bras médical.
Donc, aujourd’hui, les recommandations vont dans le sens de discuter la chirurgie dans la situation d’une récidive platine sensible et de sélectionner les patientes de façon à avoir des chances de chirurgie complète qui soient maximales. Ce qu’il est important de rappeler, c’est qu’il s’agit d’une activité de centre de recours et de centre spécialisé parce que non seulement ces chirurgies vont être complexes, les suites peuvent être compliquées, mais surtout la sélection des patientes va être difficile. En effet, il n’y a pas que le score AGO (qui comporte trois variables) qui permet de les sélectionner, il y a aussi l’état général des patientes, les effets secondaires de la première chirurgie (les patientes étaient toutes en résection complète initiale lors du traitement primaire), le fait qu’il y a déjà eu des résections digestives, les zones précédemment atteintes, le lieu de la récidive par rapport aux zones précédemment traitées… De nombreux paramètres sont à prendre en compte avant de poser une indication chirurgicale. Ces patientes, à partir du moment où elles ont été sélectionnées par le score AGO ou le score IMODEL, doivent à mon avis être référées pour réaliser l’intervention (Tab. 1-3).
Dr Frédéric Selle : À l’ère des inhibiteurs de PARP et de leur efficacité remarquable en première ligne des cancers de l’ovaire à travers les études telles que PAOLA, PRIMA ou VELIA, le dogme du résidu tumoral nul en fin d’intervention est-t-il encore plus d’actualité ou non ?
Pr Fabrice Lécuru : J’ai un peu peur de comprendre ce que tu sous-entends… c’est-à-dire que plus nous avons de médicaments à disposition et moins la chirurgie va compter ? Ce n’est bien sûr pas le cas ! Il est d’ailleurs extrêmement frustrant de ne pas avoir plus de données chirurgicales dans ces grands essais d’inhibiteurs de PARP publiés depuis un peu plus de 1 an. Je pense que c’est à méditer pour l’avenir. Néanmoins, ce qui ressort de PAOLA et PRIMA, c’est que les malades qui vont le mieux, en tout cas sur des paramètres chirurgicaux, sont celles qui bénéficient d’une résection complète en chirurgie première. Il vaut donc mieux être opérée au début qu’en intervalle, mais on n’a pas toujours le choix. De plus, les mêmes conclusions sont faites au moment de l’intervalle : une chirurgie complète est plus efficace qu’une chirurgie incomplète. Le dogme de la chirurgie complète, quand on a la réalise, reste toujours valable, y compris avec ces nouveaux médicaments. Il faut jouer toutes les cartes de la bonne façon. Donc s’il y a une indication de chirurgie première, il faut la réaliser et tout faire pour obtenir une chirurgie complète. C’était déjà la règle, et cela n’a pas changé.
Dr Frédéric Selle : Pour conclure, peux-tu nous dire quelques mots sur l’essai TRUST ?
Pr Fabrice Lécuru : Nous attendons avec impatience les résultats de TRUST qui compare la chirurgie radicale initiale à une chirurgie d’intervalle dans le cancer ovarien de stades avancés. Il va malheureusement falloir attendre encore un peu parce que je pense que nous ne les aurons pas avant au moins 2 ans. Ces résultats vont être particulièrement intéressants car, contrairement à certains essais précédents (EORTC, CHORUS, SCORPION par exemple), les patientes incluses dans cette étude sont opérables et seront prises en charge dans des centres qui ont des taux de résection complète élevés. On va donc mesurer réellement l’effet de la chirurgie. Il y a beaucoup de discussion autour de l’essai SCORPION, qui est très intéressant d’ailleurs. Il démontre qu’il n’y a pas de bénéfice, en tout cas en termes de survie, et qu’il y a plus de morbidité à faire de la chirurgie première qu’intervallaire. Cependant, la population de l’essai est une population pour laquelle, en France, nous avons une indication quasi formelle de chimiothérapie néoadjuvante. La réponse que nous attendons vraiment aujourd’hui, c’est bien celle de TRUST.
Le regard de l’oncologue médical
Pr Fabrice Lécuru : Suite aux résultats publiés de PAOLA-1 et PRIMA, quels vont être tes critères pour une indication d’inhibiteurs de PARP, du bévacizumab ou d’une association des deux ? Autrement dit, faut-il donner un inhibiteur de PARP à toutes les patientes ?
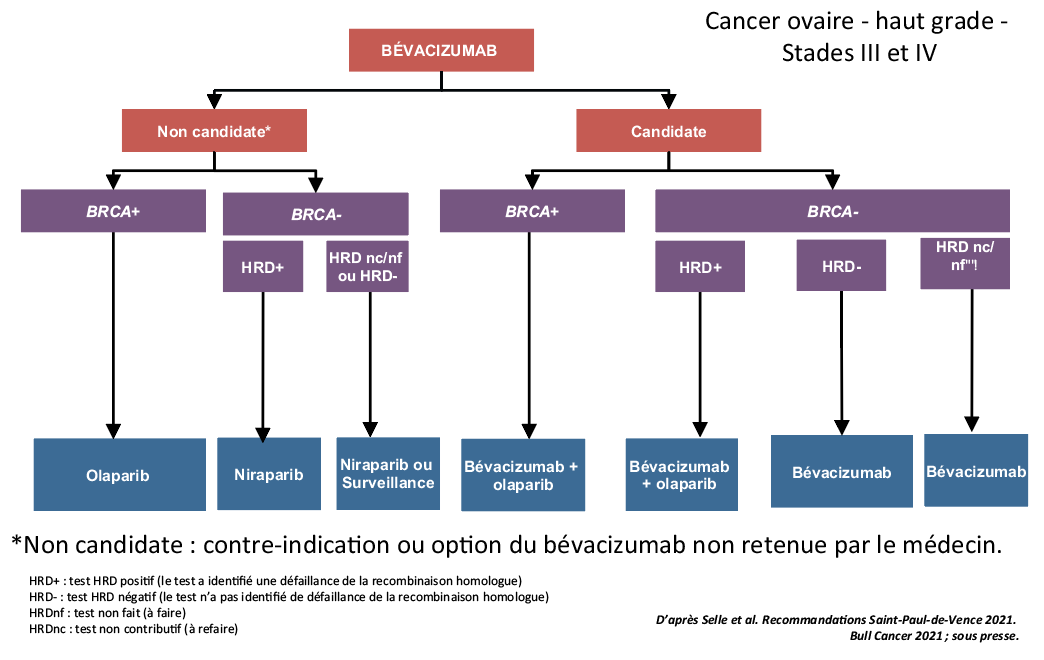
Dr Frédéric Selle : Le sujet est vaste ! À la question « faut-il un inhibiteur de PARP en 2021 à toutes les patientes qui ont un cancer de l’ovaire de stades avancés ? », ma réponse serait non. Dans un souci de médecine de précision, je pense que ce qu’il faut retenir de ces études est que l’effet thérapeutique est très significatif en termes de survie sans progression des inhibiteurs de PARP chez des patientes atteintes de cancer de l’ovaire de haut grade qui ont une défaillance de réparation de la recombinaison homologue (test HRD+). Aussi, toutes les patientes qui ont un test HRD+ doivent bénéficier d’un inhibiteur de PARP, c’est indiscutable. En revanche, pour décider du traitement médical en première ligne, il faut, tout d’abord, connaître des contingences qui sont liées aux AMM et aux remboursements de certains inhibiteurs de PARP. Je pense par exemple à l’olaparib en monothérapie chez les patientes avec une mutation BRCA germinale ou tumorale (AMM et remboursement). Il faut également tenir compte du libellé des post-ATU. Nous en avons deux qui concernent la combinaison olaparib + bévacizumab qui est destinée aux patientes HRD+ (mutation BRCA ou score d’instabilité génomique élevé sans mutation BRCA) et le niraparib qui a un libellé de la post-ATU restreint par rapport à l’AMM puisqu’il ne peut être prescrit actuellement que pour des patientes non éligibles au bévacizumab et qui ne présentent pas de mutation BRCA. Il n’a pas sa place actuellement dans cette population de patientes puisqu’il y a une alternative, qui est l’olaparib. Ainsi, à la question « quels traitements choisir ? », je renvoie aux recommandations de Saint-Paul-de-Vence (Fig. 1), en ligne sur le site Arcagy-Gineco, et qui devraient être publiées très prochainement dans le Bulletin du cancer. Plusieurs éléments participent à la décision. D’abord, il faut évoquer la place du bévacizumab. Je crois qu’il est indispensable de se poser cette première question car elle est chronologique dans le temps. En effet, l’indication du bévacizumab est la combinaison avec la chimiothérapie suivie de la maintenance alors que pour l’inhibiteur de PARP, la décision d’initier le traitement ne se prend qu’après la chimiothérapie. Il s’agit également de revenir à nos fondamentaux avant l’émergence des inhibiteurs de PARP : « quelle était la place du bévacizumab ? » sur des maladies graves. Je rappelle qu’il y a un gain de survie globale dans les stades IV dans l’étude américaine GOG218 et dans le sous-groupe dit à haut risque d’ICON7. Le deuxième point est que le bévacizumab était une première thérapie ciblée qui était fréquemment utilisée, même si les données sont moins robustes, chez les patientes qui avaient une chirurgie intervallaire, notamment quand il n’y a plus de résidu. Ces patientes avaient une maladie tellement grave initialement qu’elles ne pouvaient pas être opérées, pour lesquelles, généralement, en France, on prescrivait du bévacizumab, y compris lorsqu’elles étaient en résection complète. Sachant qu’il faut garder à l’esprit qu’il y a un certain nombre de stades IV traités par chimiothérapie première qui ont une chirurgie de Debulking sous-diaphragmatique en cas d’excellente réponse et cela reste des malades à haut risque de rechute. À mon sens, la place du bévacizumab doit être revisitée à l’issue des résultats de l’étude PAOLA chez ces patientes avec un test HDR+. Nous voyons bien que dans notre réflexion nous devons à la fois nous poser la question de la place du bévacizumab et en même temps avoir la connaissance du test HRD. Je rappelle que les recommandations de Saint-Paul-de-Vence, et notamment le groupe d’experts dédié à la thématique du testing BRCA et de la biologie moléculaire, reprécisent avec force qu’il est nécessaire pour tout cancer de l’ovaire de haut grade en première ligne de connaître le statut HRD. Savoir que la patiente est HRD+ doit lui faire bénéficier d’un inhibiteur de PARP. C’est une combinaison de ces deux réflexions qui doit nous amener à proposer un traitement.
Pr Fabrice Lécuru : Utilises-tu un inhibiteur de PARP différent selon les situations ?
Finalement, nous avons trois situations. Dans un cas, nous avons les patientes avec une mutation BRCA, pour lesquelles il y a l’olaparib en monothérapie. Concernant la place de l’association olaparib-bévacizumab chez ces patientes avec mutation BRCA, il est difficile de répondre dans la mesure où il n’y a pas eu de troisième bras olaparib seul dans PAOLA. Il n’est possible que de faire une lecture prudente comparative des études. Ce que l’on peut apercevoir, c’est que chez les patientes avec mutation BRCA, le hazard ratio dans SOLO1 et PAOLA est identique, mais le bras contrôle du bévacizumab dans l’olaparib est bien meilleur que celui de SOLO1 où il y avait du placebo. La médiane de survie sans progression dans ce bras n’était que de 13 mois. À cette lecture, on peut penser que les patientes avec mutation BRCA bénéficient aussi du bévacizumab avec une médiane de SSP de 17,7 mois dans le bras bévacizumab contrôle de l’étude PAOLA-1. Le deuxième argument qui peut être intéressant est de s’intéresser aux patientes qui étaient en réponse partielle après la séquence chirurgie-chimiothérapie, qui avaient encore une maladie résiduelle que l’on pouvait évaluer selon le taux de réponse selon RECIST ou l’élévation du CA125 (cela représentait 216 patientes sur les 806 dans PAOLA-1). On s’aperçoit que l’adjonction du bévacizumab à l’olaparib augmente de manière nette le taux de réponse, aux alentours de 64 %. On note aussi un bénéfice de 42 % en termes de taux de réponse pour le bévacizumab en monothérapie. Dans SOLO1, cette population en réponse partielle après la chimiothérapie présente un taux de réponse à l’olaparib monothérapie seulement de 24 %. Il s’agit peut-être d’un argument “indirect” en faveur de l’association olaparib-bévacizumab chez les patientes mutées BRCA. Un troisième élément de réflexion est celui d’une présentation à l’ESMO qui, par un score de pondération et de population ajustée entre celles de PAOLA-1 et de SOLO1, a montré que, avec une robustesse statistique faible (qui ne permet de faire que des hypothèses), l’association olaparib-bévacizumab serait supérieure à l’olaparib seul.
La seconde situation est la population des patientes avec un test HRD+, déficientes dans la recombinaison homologue, mais sans mutation BRCA. C’est environ 20 % des patientes dans l’étude PAOLA-1 et l’étude PRIMA. Il est évident que dans cette population il faut un inhibiteur de PARP car leur efficacité, bien que légèrement inférieure à celle des patientes avec mutation BRCA, est très nette. Quelle est l’alternative en 2021 ? Le niraparib ? C’est une option tout à fait recevable avec les résultats de l’étude PRIMA. L’association olaparib-bévacizumab est aussi une option à la lumière des analyses pré-spécifiées en sous-groupes de PAOLA-1. Dans cette situation, les deux options sont équivalentes, avec des arguments qui peuvent faire privilégier l’une plus que l’autre en fonction du stade initial de la maladie, le temps chirurgical primaire ou intervallaire et l’existence ou non d’un résidu.
La dernière situation est celle des patientes qui n’ont pas de déficience de la recombinaison homologue qui sont dites HR-proficient ou test HRD-. Il n’y a pas de bénéfice à faire de l’olaparib avec du bévacizumab dans cette population. En revanche, dans l’étude PRIMA, il y a un gain statistiquement significatif du niraparib par rapport au placebo chez ces HR-proficient, avec cependant un bénéfice clinique qu’on peut juger de très modeste (8,4 versus 5,7 mois). Là encore, on peut aussi, avec prudence, faire la lecture comparative des résultats des études. Quand on regarde le bras contrôle bévacizumab de PAOLA dans cette population, la médiane de survie sans progression est de
16 mois, un bon résultat. Je pense donc que dans cette situation le bénéfice d’un inhibiteur de PARP peut être discutable par rapport à celui du bévacizumab. D’ailleurs, c’est ce que concluent les recommandations de Saint-Paul-de-Vence. Dans cette population, il est important d’évaluer la balance bénéfices/risques en termes des commodités des traitements (oral, ambulatoire), de leur sécurité (le niraparib va nécessiter une surveillance de la numération les premières semaines), leur tolérance et aussi tenant compte des comorbidités de la patiente.
Il est évident que dans la population HRD+ non mutée BRCA il faut un inhibiteur de PARP car leur efficacité, bien que légèrement inférieure à celles des patientes avec mutation BRCA, est très nette.
Pr Fabrice Lécuru : Le test HRD est-il facile à obtenir aujourd’hui ?
Dr Frédéric Selle : Le test HRD est relativement facile à obtenir avec cependant deux conditions d’ordre technique : l’une concerne le chirurgien et la qualité des prélèvements, notamment des biopsies en cœlioscopie (avec beaucoup de matériel, évitant les électro-
coagulations et de bonnes conditions de fixation), l’autre est la qualité de sélection des lames (avec une cellularité d’au moins 20 % et au minimim de 5 mm² de surface tumorale). Le groupe des recommandations de Saint-Paul-de-Vence dédié à cette thématique a bien établi que ce circuit du testing HRD pouvait être calqué sur celui du BRCA tumoral. À savoir que le matériel est envoyé sur la plateforme de biologie moléculaire où la recherche du test BRCA tumoral est réalisée. Si celui-ci est positif, nous avons la réponse à notre question. Dans le cas contraire, du matériel doit être envoyé au laboratoire Myriad qui établira le score d’instabilité génomique (score GIS) et conclura si la patiente est HRD+ ou non. Les résultats sont alors transmis à la plateforme moléculaire et/ou au laboratoire qui les répercute aux cliniciens qui ont demandé le test. Actuellement (jusqu’à la fin de l’année 2021), ce test est mis gracieusement à disposition des prescripteurs en respectant bien le circuit. Parallèlement, il y a des développements en cours de tests académiques à l’échelon national et européen pour que l’on puisse avoir cette information pour nos patientes sans dépendre d’une industrie privée. Je rappelle que, au-delà de l’incidence thérapeutique de ce test HRD lorsqu’il est positif, nous avons une information pronostique qui est très importante pour les cliniciens. Elle est également prédictive de la réponse aux inhibiteurs de PARP ainsi que de la réponse aux platines.
Pr Fabrice Lécuru : Est-ce que l’utilisation beaucoup plus large qu’initialement des inhibiteurs de PARP en première ligne va limiter les solutions possibles lors des rechutes platine sensibles, alors que nous savons qu’ils sont un traitement très efficace, en tout cas pour les patientes mutées ?
Dr Frédéric Selle : Je ne verrais pas la problématique comme cela. En effet, compte tenu des résultats de SOLO1 et de PAOLA-1 et au vu de ce que tu nous as dit sur l’importance de la chirurgie et du résidu tumoral nul idéalement en chirurgie initiale, on voit bien qu’il faut donner le maximum de chances à nos patientes d’avoir une rémission de très longue durée, voire une guérison, c’est ce que l’on peut espérer. Je rappelle que, dans PAOLA, nous avons eu la présentation des données de PFS2 qui montrent que le gain obtenu par les inhibiteurs de PARP en première ligne se maintient jusqu’à la deuxième progression, traduisant que le gain de survie initialement obtenu avec les iPARP se prolonge au-delà de la deuxième ligne. C’est un très bon signal, je l’espère, pour un gain en survie globale. Je dirais qu’il ne faut surtout pas penser à ces patientes que l’on peut peut-être guérir à une limitation des traitements de la rechute chez celles qui sont plus favorables. Ce qui peut se discuter, c’est le cas des patientes beaucoup moins favorables, avec des résidus, y compris après chirurgie intervallaire. En fonction du test HRD, y a-t-il une priorisation à faire plutôt du bévacizumab et, à la rechute, d’envisager un inhibiteur de PARP qui entretiendrait une chimiothérapie à base de platine ou inversement ? Encore une fois, ce n’est pas dans ce sens que je le verrais. En revanche, là où tu as raison, c’est qu’il y a un certain nombre de données qui nous montrent que la réponse à la chimiothérapie après une progression sous inhibiteur de PARP est moins bonne. Cela nous invite à réfléchir à peut-être élaborer des stratégies qui contournent cette résistance en faisant appel éventuellement à d’autres combinaisons et là, il y a toute la place pour de futurs essais cliniques.
Pr Fabrice Lécuru : Certains inhibiteurs de PARP nécessitent des réductions de dose, est-ce que cela pourrait avoir un effet sur l’efficacité du traitement ?
Dr Frédéric Selle : Je dirais que le risque principal de perte d’efficacité serait les interruptions définitives de traitement. C’est important car je pense qu’il y a un devoir de repérage, d’évaluation et de traitement des effets secondaires des inhibiteurs de PARP. Lorsqu’ils sont mal repérés ou mal traités, cela peut conduire à un arrêt définitif du traitement, soit en raison d’une toxicité médicale qui ne permet pas de poursuivre ou parce que la patiente n’adhère plus au traitement. Pour moi, chez une patiente HRD+, l’arrêt d’un inhibiteur de PARP est le risque de perte d’efficacité. Alors, il y a, comme pour la chimiothérapie, dans chaque RCP des produits, des paliers de dose de réduction qui permettent de poursuivre le traitement, avec moins de toxicités. Quand on regarde un certain nombre de données, qui ne sont pas toujours publiées, et que l’on se pose la question : « est-ce qu’il y a un maintien du gain de la PFS en fonction de la dose reçue ? » Il semble que oui. Pour niraparib par exemple, la posologie initiale théorique est de 300 mg avec un amendement, depuis l’étude RADAR, d’ajustement de la dose individualisé (commencer à 200 mg pour les patientes qui font moins de 77 kg et/ou avec moins de 150 000 plaquettes) pour une moindre toxicité. Depuis, il y a eu la présentation de l’étude NORA à l’ESMO 2020. Il s’agissait d’un essai avec près de 300 patientes en rechute platine sensible qui comparait le niraparib à un placebo. En termes de PFS, on retrouve les mêmes résultats que NOVA montrant un bénéfice comparable. Dans cette étude, toutes les patientes ont commencé la dose de manière individualisée. Il semblerait donc que l’efficacité ne soit pas altérée pour le niraparib à débuter à 200 mg. Il faut retenir qu’il existe des effets secondaires qui nécessitent des paliers de réduction de dose et j’invite les prescripteurs à les respecter. L’objectif est tout de même de maintenir ce traitement qui est très important pour ces patientes.
Propos recueillis par Marianne Carrière
Fabrice Lécuru déclare avoir des liens d’intérêt avec GSK, AstraZeneca. Frédéric Selle déclare avoir les liens d’intérêt avec GSK, MSD, AstraZeneca, Roche.