Le diabète fait partie des maladies les plus fréquentes et dont la prévalence augmente le plus rapidement au monde. Non pris en charge, il fait encourir un risque d’insuffisance de divers organes et augmente donc la morbi-mortalité (1). Or nombre de traitements peuvent affecter l’équilibre du diabète. Connus depuis les années 1940, les glucocorticoïdes font partie des traitements les plus largement utilisés pour contrôler les maladies inflammatoires, auto-immunes ou cancéreuses (en parallèle d’une chimiothérapie ou adjuvant à une neurochirurgie), et leurs effets secondaires, notamment métaboliques, sont non négligeables (2). Ces derniers peuvent même être à l’origine de diabètes de novo, alors appelés diabètes cortico-induits.
Dans l’étude de Donihi et al., étudiant les patients hospitalisés en médecine interne générale, environ 11 % de l’ensemble des patients étaient traités par hautes doses de glucocorticoïdes (> 40 mg de prednisone/jour pendant au minimum plus de 48 heures), et 64 % d’entre eux ont développé au moins un épisode d’hyperglycémie et près de la moitié un diabète (3). En outre, plusieurs cas de comas acidocétosiques ou hyperosmolaires ont été relevés dans la littérature, dont certains ayant entraînés le décès (3).
L’enjeu est alors de pouvoir suivre l’augmentation des besoins en insuline au cours de ces traitements.
Physiopathologie impliquée
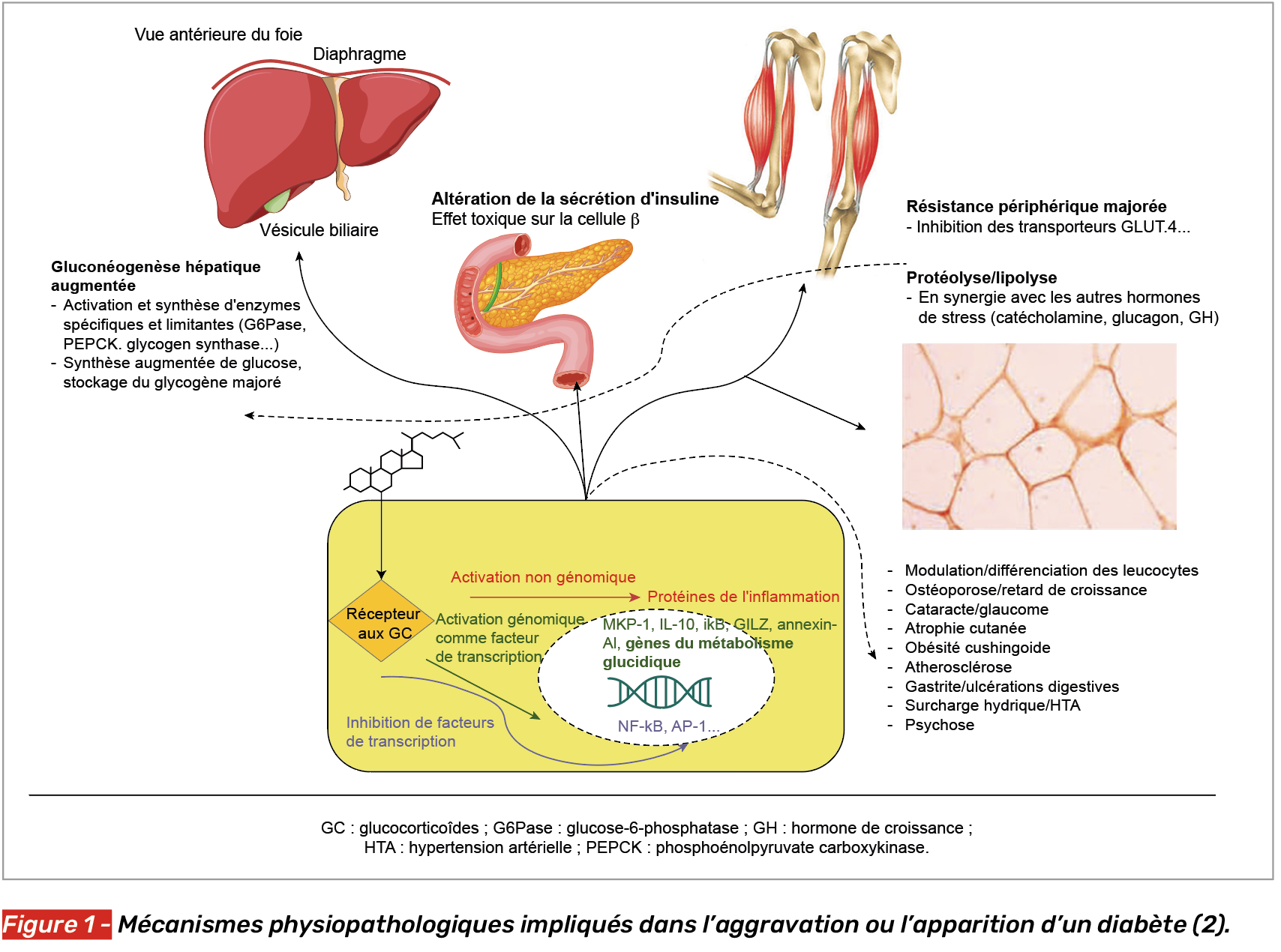
L’effet des glucocorticoïdes sur le métabolisme glucidique a bien été démontré. Ils vont entraîner une dysrégulation glycémique par plusieurs voies (Fig. 1). Ils créent en effet une augmentation de la néoglucogenèse hépatique, mais également une protéolyse, une lipolyse et une insulinorésistance périphérique, et sont directement impliqués dans une atteinte de la cellule β du pancréas (4-6).
Il est toutefois important de noter que l’hyperglycémie induite par les stéroïdes peut ne pas être remarquée par le clinicien du fait qu’ils affectent beaucoup plus la glycémie post-prandiale que la glycémie à jeun prise avant le soin (7).
Bien veiller donc à la surveillance de la glycémie avant repas et 2 h après. Une glycémie comprise entre 100 et 126 mg/dl indique une hyperglycémie à jeun, et une glycémie post-prandiale comprise entre 141 et 199 mg/dl indique une intolérance au glucose. Au-delà, on peut poser le diagnostic de diabète (8).
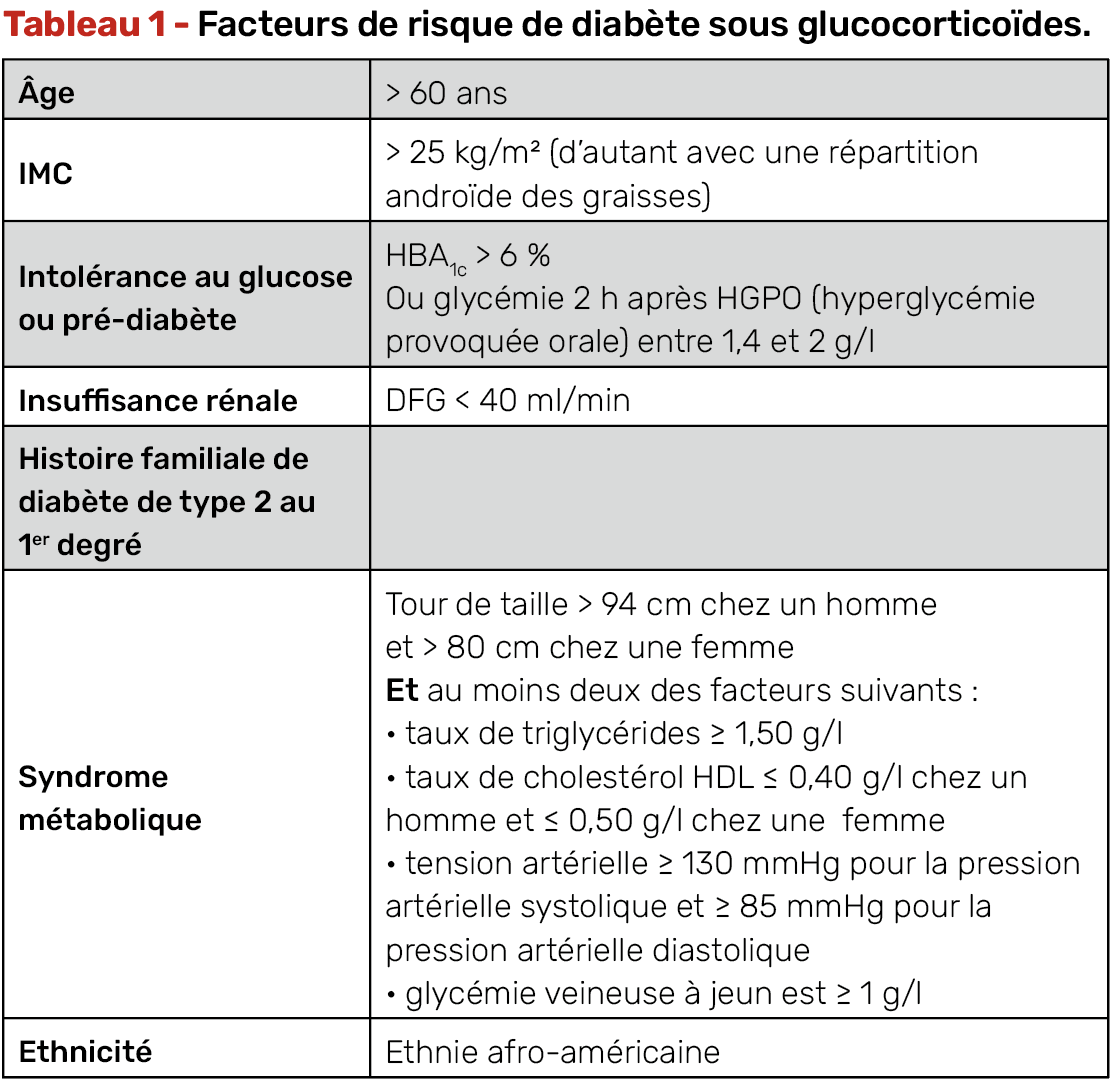
Facteurs de risque de diabète de novo ou de déséquilibre glycémique majeur (Tab. 1)
• Dans la revue de Clore et al. (9), la dose totale de glucocorticoïdes et la durée du traitement ont été retrouvées comme de puissants facteurs prédictifs de l’apparition ou de la dégradation significative d’un diabète.
• L’âge et l’indice de masse corporelle (IMC) constituent d’autres facteurs de risque.
• De plus, l’anamnèse familiale positive pour un diabète, une insuffisance rénale et une intolérance au glucose préexistante a été aussi évoquée (2, 10).
• Enfin, il a été démontré que les variations génétiques trouvées dans la population sont utiles pour prédire les réponses métaboliques à la thérapie aux glucocorticoïdes qui sont uniques à chaque individu (11).
Quelle prise en charge proposer ?
Il n’y a pas de consensus bien établi, mais uniquement des opinions d’experts. De façon générale, un traitement va pouvoir être proposé au patient où l’on va devoir le réadapter lorsque les glycémies dépassent 1,4 g/l avant repas et 2 g/l en post-prandial sur plusieurs jours consécutifs.
Chez les patients diabétiques, il peut être conseillé :
• d’intensifier le traitement antidiabétique,
• d’instaurer une insulinothérapie, si elle n’est pas déjà en place,
• ou d’augmenter la dose d’insuline si elle est déjà administrée,
avant même de commencer un traitement par glucocorticoïdes. Le traitement est bien sûr à adapter à chaque patient.
Les antidiabétiques oraux
Les antidiabétiques oraux sont cependant majoritairement insuffisants pour obtenir un contrôle glycémique satisfaisant, en particulier dans les situations d’administration prolongée de glucocorticoïdes à moyenne et forte doses. Mais, dans le cadre d’une corticothérapie au long cours ou d’un authentique diabète de novo cortico-induit, la metformine est à privilégier en l’absence de contre-indication, car elle est la seule molécule luttant contre l’insulinorésistance et ne provoque pas de risque d’hypoglycémie (11).
L’insulinothérapie
La plupart des patients nécessiteront ainsi une insulinothérapie (adaptée au poids) avec une surveillance glycémique et un ajustement régulier (2). Il convient de noter que les patients peuvent nécessiter des doses plus élevées d’insuline prandiale/rapide que d’insuline basale au vu de la pharmacocinétique des glucocorticoïdes (12, 13). De plus, il est important de rappeler que la suppression du cortisol endogène peut accroître la susceptibilité à l’hypoglycémie nocturne (14).
Choix de l’insuline
Concernant le choix du type d’insuline à utiliser, il n’a pas été retrouvé d’avantages à l’utilisation de l’insuline NPH (intermédiaire) par rapport à l’insuline glargine ou détémir (dite lente) (13).
Il est ainsi recommandé de débuter par la mise en place d’une insulinothérapie basale seule le matin, avec protocole de correction par insuline rapide si besoin, puis de réévaluer dans un second temps avant un changement au profit d’un schéma basal-bolus (12).
En pratique
Dès la mise en route d’une insulinothérapie, penser à la prescription d’une autosurveillance glycémie continue via capteurs à poser au bras et/ou au ventre pour améliorer l’adhérence thérapeutique au traitement et mieux monitorer les doses d’insuline par la suite.
La dose initiale courante d’insuline basale est de 0,2 UI/kg, la valeur la plus élevée étant retenue. La dose est ensuite ajustée en fonction du résultat de la glycémie matinale entre autres (7).
Les règles hygiéno-diététiques
D’autre part, il s’agira également en parallèle d’orienter le patient vers une amélioration de ses règles hygiéno-diététiques si nécessaire. Par conséquent, privilégier une activité physique régulière ou la renforcer avec une alimentation équilibrée ou la plus équilibrée possible (par exemple en supprimant/limitant fortement les aliments à index glycémique élevé tels que les boissons sucrées, le sucre). Une consultation diététique dédiée est souvent nécessaire.
L’auteure déclare ne pas voir de liens d’intérêt en rapport avec cet article.
Bibliographie
1. Chen X, Zhang L, Chen W. Global, regional, and national burdens of type 1 and type 2 diabetes mellitus in adolescents from 1990 to 2021, with forecasts to 2030: a systematic analysis of the global burden of disease study 2021. BMC Med 2025 29 ; 23 : 48.
2. Genolet P, Petignat P, Petite C. Diabète cortico-induit, une entité fréquente sans prise en charge standardisée. Rev Med Suisse 2012 ; 336 : 800-5.
3. Donihi AC, Raval D, Saul M et al. Prevalence and predictors of corticosteroid-related hyperglycemia in hospitalized patients. Endocr Pract 2006 ; 12 : 358-62.
4. McMahon M, Gerich J, Rizza R. Effects of glucocorticoids on carbohydrate metabolism. Diabetes Metab Rev 1988 ; 4 : 17-30.
5. Van Raalte DH, van Genugten RE, Linssen MM et al. Glucagon-like peptide-1 receptor agonist treatment prevents glucocorticoid-induced glucose intolerance and islet-cell dysfunction in humans. Diabetes Care 2011 ; 34 : 412-7.
6. Schacke H, Docke WD, Asadullah K. Mechanisms involved in the side effects of glucocorticoids. Pharmacol Ther 2002 ; 96 : 23-43.
7. Oyer DS, Shah A, Bettenhausen S. How to manage steroid diabetes in the patient with cancer. J Support Oncol 2006 ; 4 : 479-83.
8. Oyer DS, Shah A, Bettenhausent S. How to manage steroid diabetes in the patient with cancer. J Support Oncol 2006 ; 4 : 479-83.
9. Clore JN, Thurby-Hay L. Glucocorticoid-induced hyperglycemia. Endocr Pract 2009 ; 15 : 469-74.
10. Oğuz SH. Management of glucocorticoid-induced diabetes. Acta Medica 2024 ; 55 : 17-21.
11. Hu W, Jiang C, Kim M et al. Individual-specific functional epigenomics reveals genetic determinants of adverse metabolic effects of glucocorticoids. Cell Metab 2021 ; 33 : 1592-609.
12. Li JX, Cummins CL. Fresh insights into glucocorticoid-induced diabetes mellitus and new therapeutic directions. Nat Rev Endocrinol 2022 ; 18 : 540-57.
13. Tatalovic M, Lehmann R, Cheetham M et al. Management of hyperglycaemia in persons with non-insulin-dependent type 2 diabetes mellitus who are started on systemic glucocorticoid therapy: A systematic review. BMJ Open 2019 ; 9 : e028914.
14. Descours M, Rigalleau V. Glucocorticoid-induced hyperglycemia and diabetes: Practical points. Ann Endocrinol 2023 ; 84 : 353-6.


