L’essentiel en un clin d’œil
Les résultats obtenus à l’aide d’essais cliniques randomisés dont la méthodologie est robuste ont été mis avant dans ce Top 5 ASCO 2023.
• L’essai D-TORCH a montré que le gel de diclofénac était très efficace en matière de prévention du syndrome main-pied associé à la capécitabine.
• L’essai REMEMBER n’a pas montré d’efficacité du donépézil, un inhibiteur de l’acétylcholine estérase indiqué dans le traitement symptomatique de la maladie d’Alzheimer, dans le traitement des troubles cognitifs liés au cancer et à ses traitements chez les patientes suivies pour un cancer du sein en rémission.
• Le programme NeuroCARE, une intervention s’intéressant à l’anxiété chez les aidants de patients atteints de tumeurs malignes cérébrales primitives, a montré, dans un essai contrôlé randomisé, une diminution significative des symptômes d’anxiété et de dépression, un meilleur sentiment d’efficacité perçu et un meilleur sentiment de capacité d’adaptation chez les aidants.
• L’essai BWEL a évalué, versus groupe témoin, l’effet d’un programme réalisé au téléphone en faveur de la promotion de la perte de poids (Weight Loss Intervention (WLI)). Ce programme a permis une perte de poids statistiquement et cliniquement significative chez les patients atteints de cancer du sein en surpoids ou obèses.
• Enfin, un essai randomisé, évaluant le yoga versus placebo comportemental, a montré que les patients de plus de 60 ans en rémission d’un cancer peuvent pratiquer le yoga en toute sécurité, et que cette pratique permet d’améliorer la fatigue, la qualité de vie globale et sa composante émotionnelle.
TOP 1 – Un nouveau standard dans la prévention du syndrome main-pied lié à la capécitabine (résultats de D-TORCH)
Le syndrome main-pied (SMP) induit par la capécitabine est associé à une détérioration de la qualité de vie des patients, de plus la dose de capécitabine est souvent réduite pour gérer cet événement indésirable. Le célécoxib est l’un des rares traitements efficaces pour prévenir ce SMP, mais les risques cardiovasculaires et de saignements digestifs doivent être pris en compte, son utilisation en prévention est alors limitée.
Un essai contrôlé randomisé a été mené en double aveugle afin d’évaluer le diclofénac topique versus placebo dans la prévention du SMP chez les patients recevant de la capécitabine.
L’essai D-TORCH
Les patients atteints de cancers du sein et gastro-intestinaux (GI) devant recevoir un traitement par capécitabine (monothérapie ou association) ont été randomisés en 1:1 pour recevoir du diclofénac topique (1 g sur chaque main x 2 par jour) ou un gel placebo pendant quatre cycles ou jusqu’au développement d’un SMP. La randomisation était stratifiée (homme ou femme ; capécitabine en monothérapie ou thérapie associée).
L’objectif principal était de montrer que la fréquence d’apparition du SMP de grades ≥ 2 était inférieure dans le groupe diclofénac topique par rapport au groupe placebo.
Les résultats
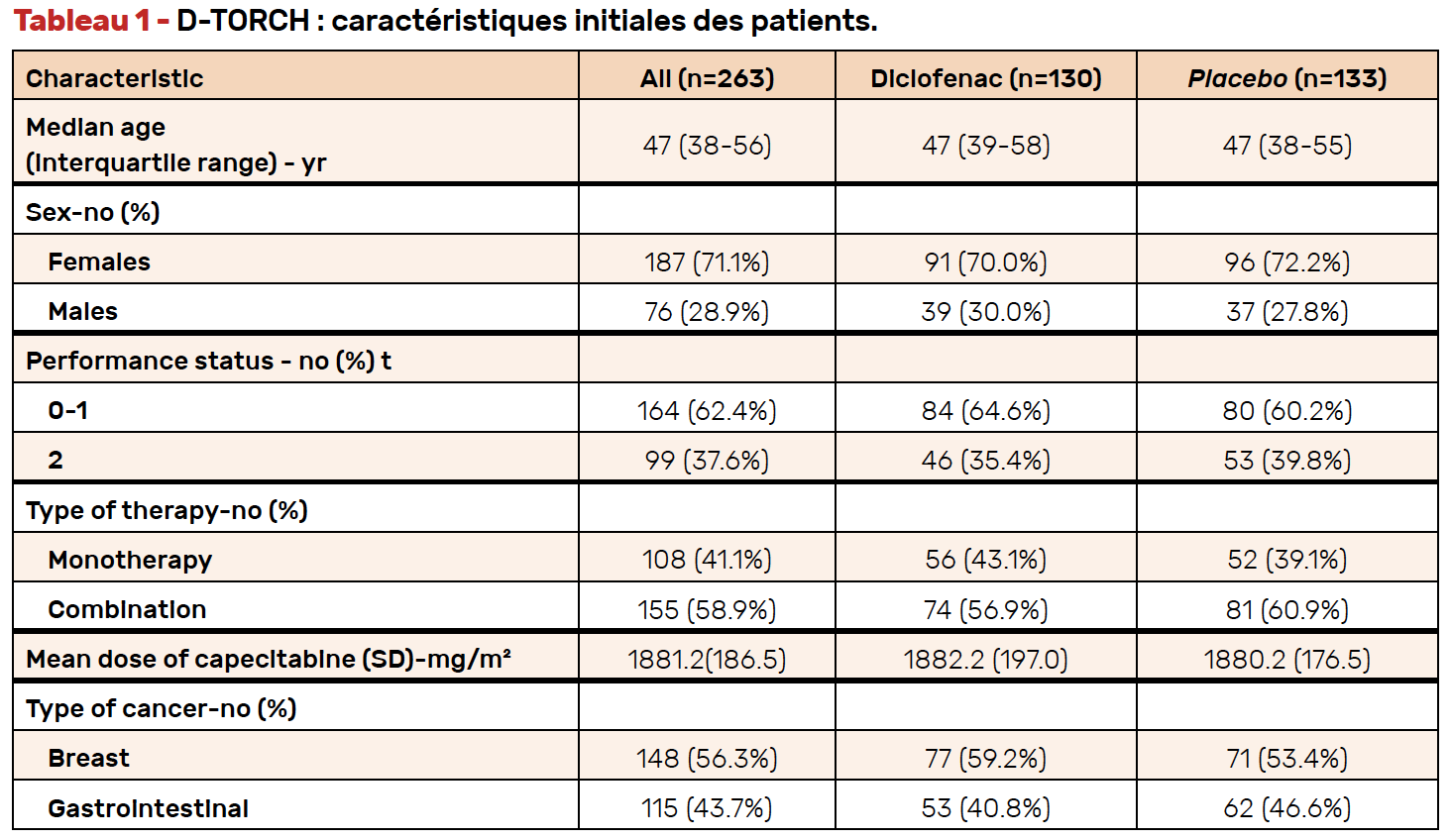
Un total de 263 patients a été randomisé : gel de diclofénac topique (n = 130) ou un placebo (n = 133). Les caractéristiques des patients étaient similaires dans les deux bras (Tab. 1).
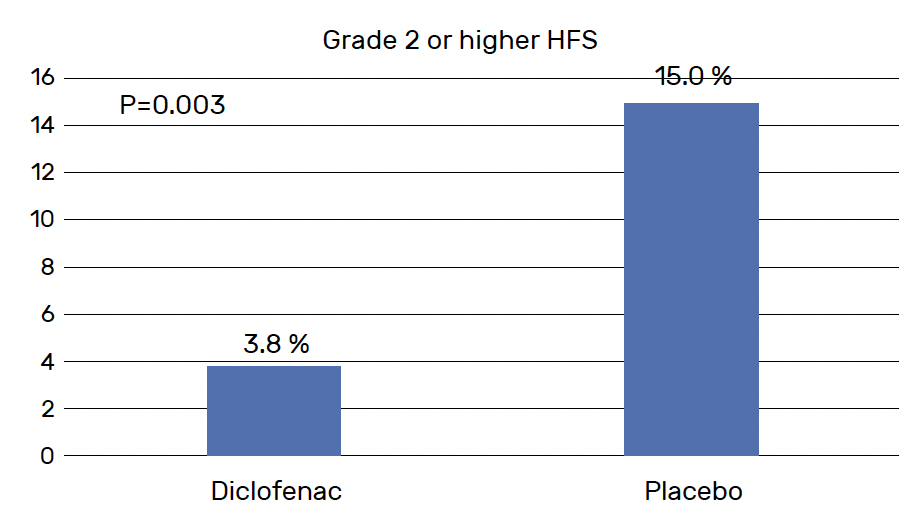
La fréquence d’apparition du SMP de grades ≥ 2 était de 3,8 % (IC 95 % = 1,6-8,9 %) dans le bras diclofénac, contre 15,0 % (IC 95 % = 9,9-22,2 %) dans le bras placebo
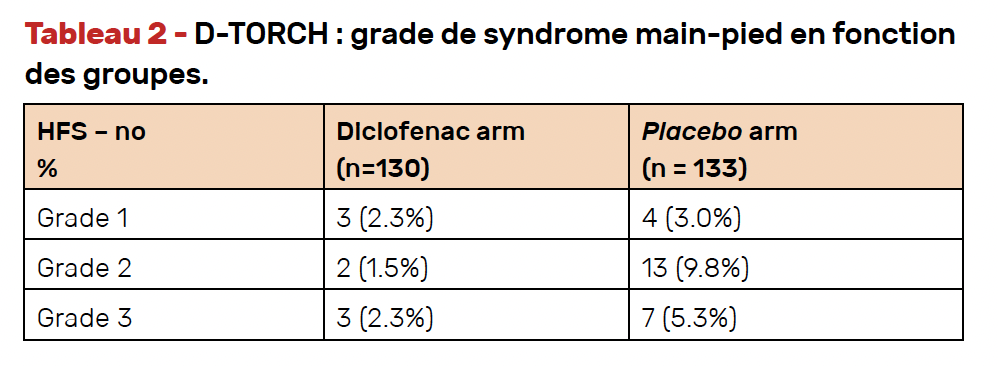
(p = 0,003) (Fig. 1). La fréquence d’apparition du SMP tous grades (Tab. 2) était aussi significativement plus faible dans le bras intervention (6,1 versus 18,1 % ; p = 0,003). Les réductions de dose de capécitabine étaient moins fréquentes dans le bras diclofénac (3,8 %) que dans le bras placebo (15 %) (p = 0,002).
Figure 1 – D-TORCH : fréquence d’apparition du syndrome main-pied de grades ≥ 2 en fonction des groupes.
À retenir
Les auteurs concluent que le gel de diclofénac est efficace pour prévenir le SMP chez les patients recevant de la capécitabine et a également été associé à des réductions moins fréquentes de la dose de capécitabine. Cet essai permet au gel de diclofénac de devenir le nouveau standard en matière de prévention du SMP associé à la capécitabine.
• Santhosh A, Batra A, Kumar A et al. Randomized double-blind, placebo-controlled study of topical diclofenac in prevention of hand-foot syndrome in patients receiving capecitabine. J Clin Oncol 2023 ; 41 : abstr. 12005.
TOP (FLOP) 2 – Absence d’efficacité du donépézil dans le traitement des troubles cognitifs tardifs liés au cancer (résultats de l’essai REMEMBER)
Les troubles cognitifs liés au cancer et à ses traitements (TCLC) sont fréquents chez les survivantes du cancer du sein. Des données suggèrent que certains médicaments, comme le donépézil, indiqué dans le traitement symptomatique de la maladie d’Alzheimer, pourraient être efficaces dans les TCLC.
L’essai clinique randomisé en double aveugle contre placebo REMEMBER a évalué l’efficacité de donépézil, un inhibiteur de l’acétylcholine estérase, afin de réduire les TCLC tardifs chez les patientes survivantes d’un cancer du sein et précédemment exposées à une chimiothérapie.
L’essai REMEMBER
Il a inclus des femmes de 18 ans et plus avec un antécédent de cancer du sein traitées par au moins quatre cycles de chimiothérapie de 1 à 5 ans avant l’inclusion, et qui présentaient une perturbation du test d’apprentissage verbal de Hopkins (HVLT-R). Ce test consiste en la mémorisation d’une liste de mots. Il évalue la capacité de rappel immédiatement de cette liste de mots (rappel immédiat) et après 20 minutes (rappel différé).
Les femmes étaient ensuite randomisées pour recevoir un traitement de 24 semaines de donépézil (5 mg/jour x 6 semaines titré à 10 mg/jour x 18 semaines) ou un placebo. Une batterie de tests évaluant la mémoire, l’attention, la fonction exécutive, la fluidité verbale et la vitesse de traitement a été administrée au départ et après 12, 24 et 36 semaines.
Les résultats
Un total de 276 femmes a été randomisé (âge moyen 57,1 ans ; SD = 10,5) pour recevoir donépézil (n = 140) ou placebo (n = 136), en moyenne à 29,6 mois après la fin de la chimiothérapie.
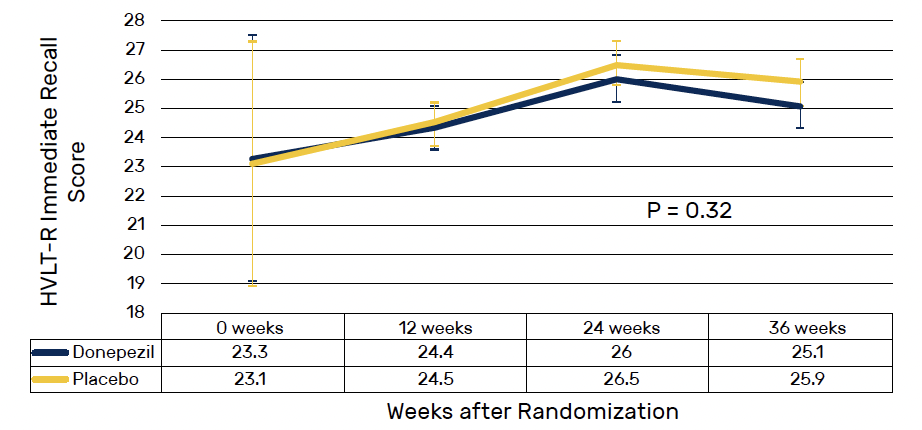
Le critère principal de jugement était le score HVLT-R total à 24 semaines, il n’était pas différent entre les deux groupes (moyenne 25,98 et 26,50 respectivement pour donépézil et placebo ; p = 0,32) (Fig. 2). Il n’y avait pas non plus de différence significative entre les traitements à 12, 24 ou 36 semaines sur l’attention, la fonction exécutive, la fluidité verbale ou la vitesse de traitement. Les analyses exploratoires ajustant les résultats bruts sur le niveau d’éducation, la fatigue et la dépression n’ont également montré aucune différence entre les groupes.
Figure 2 – REMEMBER : score HVLT-R total en fonction du groupe donépézil ou placebo.
À retenir
Le donépézil n’est pas efficace dans le traitement des TCLC survenant chez les patientes survivantes d’un cancer du sein 1 à 5 ans après la fin de la chimiothérapie.
• Rapp SR, Van Meter Dressler E, Brown WM et al. Phase 3 randomized placebo-controlled trial of donepezil for late cancer-related cognitive impairment in breast cancer survivors exposed to chemotherapy from the Wake Forest NCORP Research Base REMEMBER trial (WF97116). J Clin Oncol 2023 ; 41 : abstr. 12004.
TOP 3 – La télémédecine au service de la santé des aidants principaux de patients atteints de tumeurs malignes cérébrales primitives
Dans une précédente étude, il a été montré que les aidants qui prennent en charge des patients atteints de tumeurs malignes cérébrales primitives (TMCP) sont confrontés à des difficultés lorsque la maladie évolue. Notamment, plus de 50 % de ces aidants présenteraient des symptômes cliniquement significatifs d’anxiété. Cette pression exercée sur les aidants était, de plus, associée à une plus mauvaise survie des patients.
Un essai contrôlé randomisé a évalué l’efficacité du programme NeuroCARE, une intervention spécifique s’intéressant à l’anxiété chez les aidants.
L’essai
Les personnes éligibles devaient être aidants d’un patient atteint de TMCP depuis au moins 6 mois et devaient présenter des symptômes d’anxiété cliniquement significatifs (score ≥ 5 au Generalized Anxiety Disorder-7 (GADS-7)). Les aidants participants étaient alors randomisés 1:1 dans le bras intervention (NeuroCARE) ou le bras “soins habituels”.
Le programme NeuroCARE consistait en six séances individuelles de télésanté avec un clinicien en santé mentale pour former les participants à :
1) faire face à l’inquiétude ;
2) utiliser des techniques de communication positives ;
3) optimiser le soutien social ;
4) favoriser la relaxation et le sommeil sain.
Les participants ont rempli des questionnaires au début de l’étude, immédiatement après l’intervention (à 11 semaines) et à 16 semaines.
Le critère de jugement principal était les symptômes d’anxiété à 11 semaines (score d’anxiété de la Hospital Anxiety and Depression Scale (HADS)). Les autres évaluations étaient les symptômes de la dépression (score de dépression de la HADS), la qualité de vie (Caregiver QOL survey), le fardeau des aidants (Caregiver Reaction Assessment), le sentiment d’efficacité personnelle perçue (échelle de Lewis), les mesures d’adaptation (coping) (Measure of Current Status) et les symptômes de stress post-traumatique (SSPT).
Une analyse de covariance a été utilisée pour comparer l’efficacité de NeuroCARE par rapport aux soins habituels.
Les résultats
Au total, 120 aidants ont été inclus (60 dans chaque bras, âge moyen = 53 ans, 83 % de femmes). La majorité d’entre eux s’occupaient de leur conjoint/partenaire (70 %), de leur enfant (17 %) ou de leur parent (7 %).
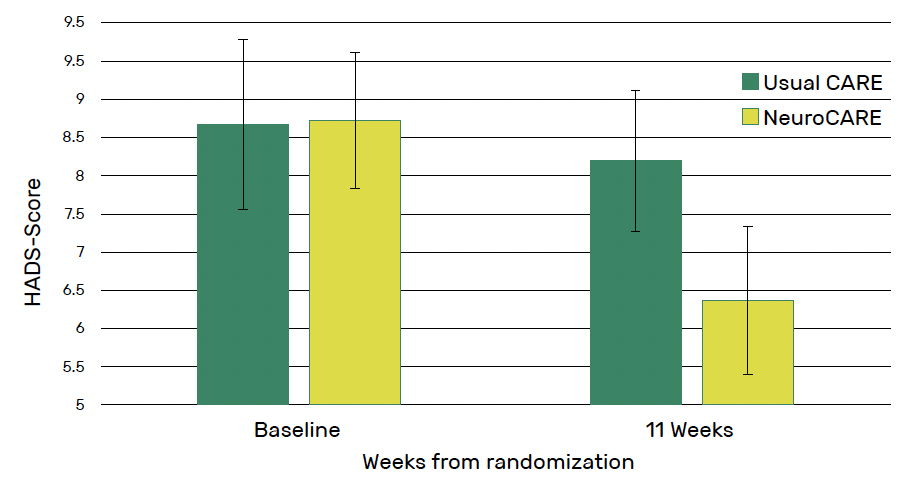
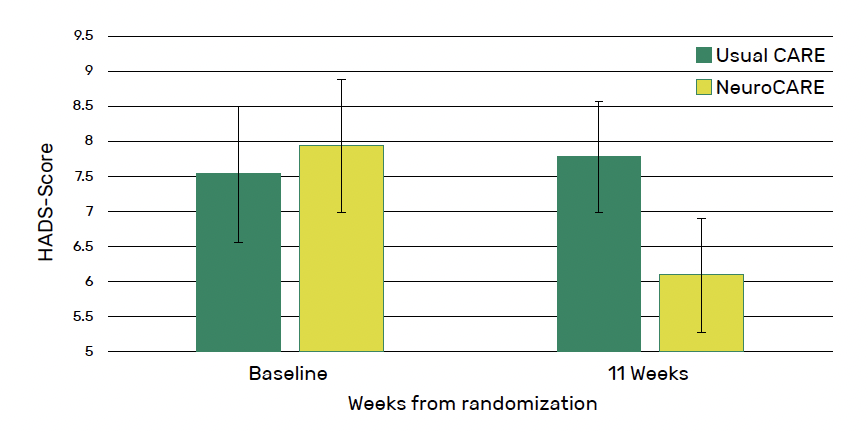
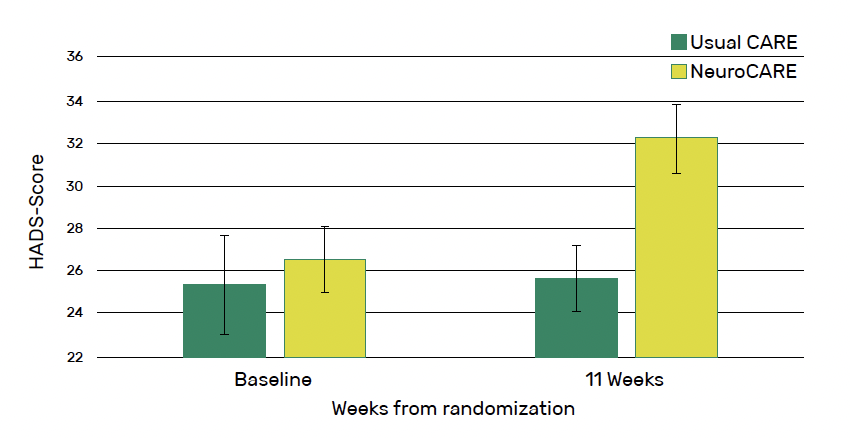
À 11 semaines, les participants à NeuroCARE ont signalé des symptômes d’anxiété significativement plus faibles que ceux du bras soins habituels (moyenne : 8,87 contre 10,69 ; p = 0,008). Ils ont également signalé des symptômes de dépression significativement plus faibles (6,08 versus 7,77 ; p = 0,004), un plus grand sentiment d’efficacité personnelle perçue (128,81 versus 111,17 ; p < 0,001) et un meilleur sentiment de capacité d’adaptation (32,25 versus 25,65 ; p < 0,001) (Fig. 3, 4 et 5).
Figure 3 – NeuroCARE : évolution des symptômes d’anxiété entre baseline et 11 semaines.
Figure 4 – NeuroCARE : évolution des symptômes de dépression entre baseline et 11 semaines.
Figure 5 – NeuroCARE : évolution du sentiment de capacité d’adaptation (coping) entre baseline et 11 semaines.
À retenir
Cette intervention en télésanté (NeuroCARE) a permis notamment une diminution significative des symptômes d’anxiété et de dépression, un meilleur sentiment d’efficacité perçue et un meilleur sentiment de capacité d’adaptation chez les aidants de patients atteints de TMCP.
• Forst DA, Podgurski AF, Strander SM et al. Telehealth-based psychological intervention for caregivers of patients with primary malignant brain tumors: A randomized controlled trial.. J Clin Oncol 2023 ; 41 : abstr. 12008.
TOP 4 – La télémédecine au service de la lutte contre le surpoids et l’obésité (résultats de l’essai BWEL)
L’obésité est un facteur de mauvais pronostic connu dans le cancer du sein. L’essai Breast Cancer Weight Loss (BWEL) a évalué l’effet d’un programme réalisé au téléphone en faveur de la promotion de la perte de poids (Weight Loss Intervention (WLI)) sur la survie sans maladie invasive chez les patientes atteintes d’un cancer du sein.
L’essai BWEL
Les critères d’éligibilité étaient :
• diagnostic de cancer du sein dans les 14 mois précédant l’inclusion (HER2 négatif, stade 2-3),
• chimiothérapie et radiothérapie (si administrées) terminées,
• indice de masse corporelle (IMC) > 27 kg/m2.
Les patientes étaient randomisées 1:1 dans le groupe WLI ou dans le groupe témoin.
Le programme proposé pour la perte de poids était dispensé par téléphone. Il est fondé sur la théorie sociale cognitive et adapté des programmes de prévention en diététique (LISA ou Look AHEAD). Les sujets recevaient un total de 42 appels en 2 ans par un coach dédié.
L’objectif était de perdre 10 % de poids, de baisser les apports caloriques alimentaires et d’encourager l’activité physique.
La taille et le poids ont été mesurés au départ puis à 12 mois. L’analyse statistique a été réalisée avec des modèles de régression univariés et multivariés.
Les résultats
Au total, 3 181 femmes ont été randomisées entre août 2016 et février 2021. L’âge était en moyenne de 53,4 (± 10,58) ans, 57 % des patientes étaient ménopausées au moment du diagnostic. À baseline, l’IMC moyen était de 34,5 (± 5,74) kg/m2.
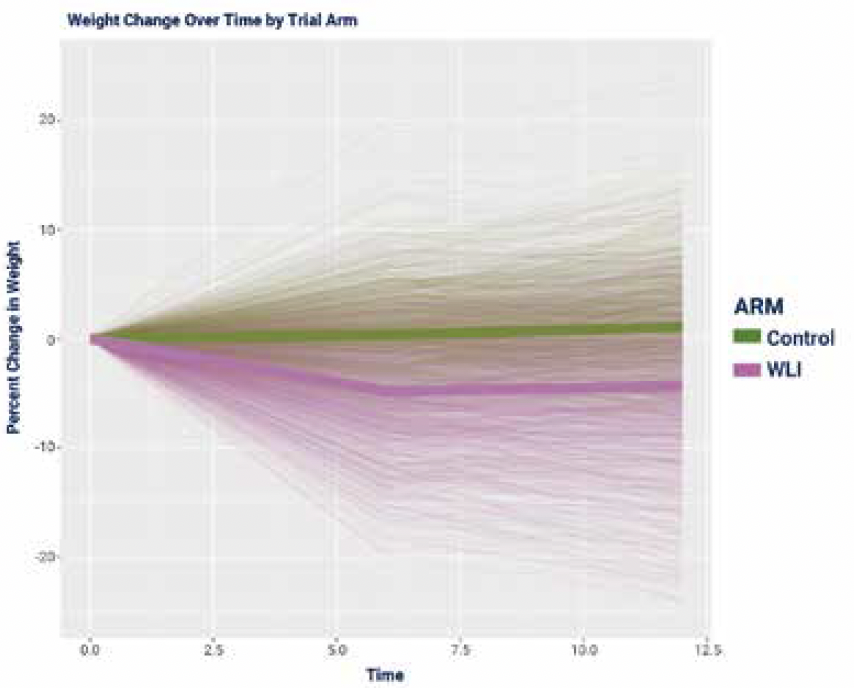
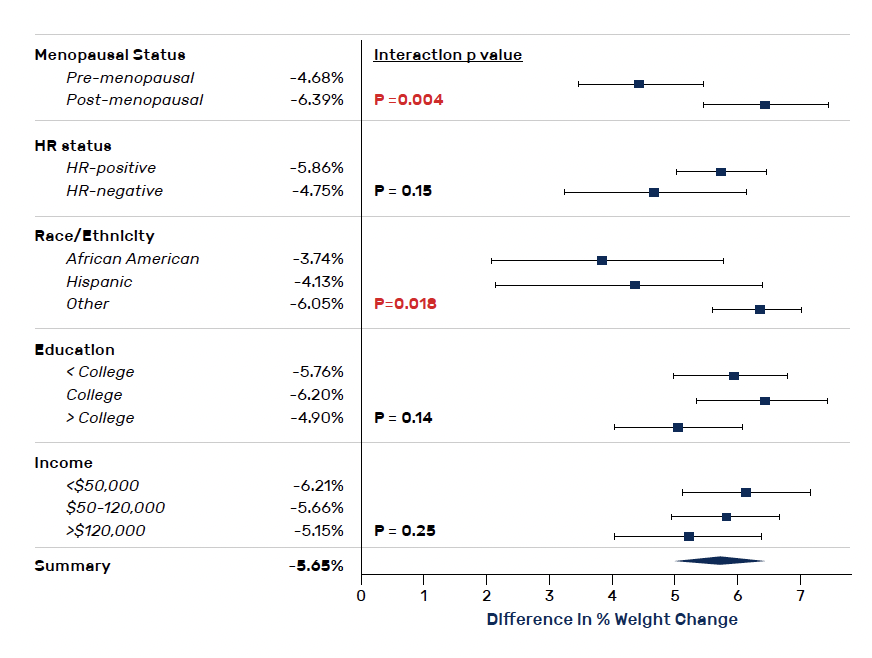
Les patientes du groupe WLI ont vu une diminution significative du poids par rapport aux témoins. Les patientes du groupe intervention ont perdu en moyenne 4,8 % (± 7,9) de poids corporel initial à 12 mois, et les patientes du groupe témoins ont augmenté de 0,8 % (± 6,4) de poids corporel (p < 0,0001) (Fig. 6). L’effet du programme WLI différait significativement selon le statut ménopausique (p test d’interaction = 0,0057), mais pas le statut Récepteur Hormonal (HR) (p test d’interaction = 0,17) (Fig. 7).
Figure 6 – BWEL : évolution du poids au cours du temps en fonction du groupe entre baseline et 11 semaines.
Figure 7 – BWEL : analyse de sous-groupes.
À retenir
Le programme WLI par téléphone a permis une perte de poids cliniquement significative chez les patientes atteintes de cancer du sein en surpoids ou obèses. L’effet sur la survie sans maladie invasive fait l’objet d’un suivi prospectif des patientes incluses et fera l’objet de futures communications.
• Ligibel JA, Ballman KV, McCall LM et al. Effect of a telephone-based weight loss intervention (WLI) on weight at 12-months in women with early breast cancer: Results from the Breast Cancer Weight Loss (BWEL) trial. J Clin Oncol 2023 ; 41 : abstr. 12001.
TOP 5 – Le yoga améliore la fatigue et la qualité de vie (dans un essai randomisé versus placebo comportemental)
Les patients suivis pour un cancer en rémission présentent fréquemment une fatigue chronique et souhaitent des moyens pour lutter contre celle-ci, notamment les plus âgés d’entre eux.
L’objectif de cet essai était d’étudier l’efficacité du yoga par rapport à un placebo comportemental pour améliorer la fatigue et la qualité de vie chez les patients âgés en rémission.
L’étude
Les patients en rémission d’un cancer (2 à 60 mois après le traitement) âgés de 60 ans et plus ont été randomisés pour recevoir Yoga for Cancer Survivors (YOCAS) ou un placebo comportemental (Survivorship Health Education (SHE)) pour des séances de 75 minutes deux fois par semaine pendant 4 semaines. Le YOCAS comprend des exercices de respiration, des poses de yoga et des activités en pleine conscience. Le SHE (groupe placebo) comprend une éducation fondée sur les recommandations de l’ASCO en matière de survie au cancer.
La fatigue et la qualité de vie ont été évaluées avant et après l’intervention à l’aide de l’échelle FACIT-F (Functional Assessment for Chronic Illness Therapy-Fatigue). L’analyse statistique a été réalisée à l’aide d’ANCOVA.
Les résultats
Au total, 173 patients ont été inclus (91 % de femmes, âge moyen de 67 ans [60-85], 71 % de cancer du sein). En moyenne, les participants ont participé à 183 minutes de yoga/semaine (séances en présentiel et à domicile). Il n’y avait pas d’effets indésirables liés à l’intervention.
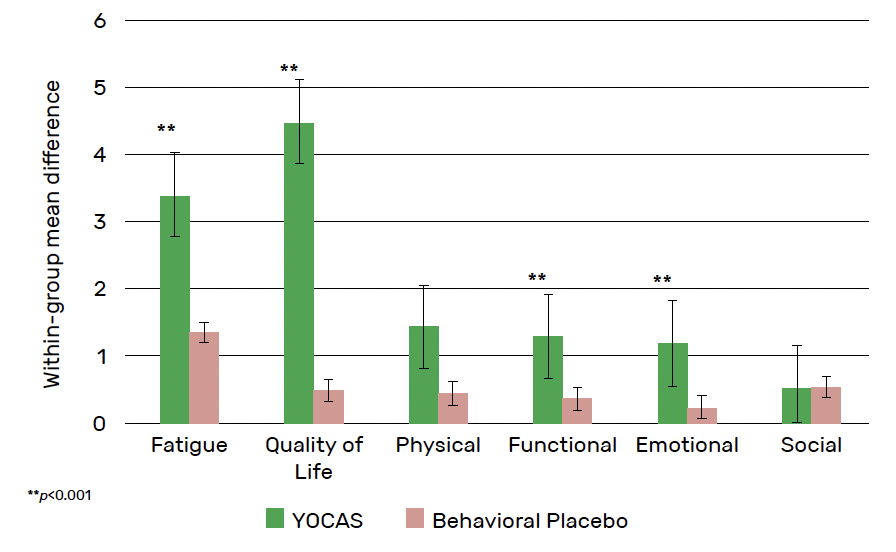
Il a été noté des différences significatives entre les groupes sur la fatigue. Les participants du groupe YOCAS ont noté une amélioration significativement plus importante de la fatigue que les témoins (1,6 ± 0,9 ; p < 0,05). Il y avait également des différences significatives sur la composante émotionnelle de la qualité de vie (0,8 ± 0,4 ; p < 0,045) et sur la qualité de vie globale (3,8 ± 1,4 ; p < 0,007). Les résultats sont synthétisés dans la figure 8.
Figure 8 – YOCAS : résultats principaux de l’intérêt du programme.
Il y avait enfin des différences (non statistiquement significatives) sur les composantes physique et fonctionnelle de la qualité de vie (respectivement 0,8 ± 0,4 ; p < 0,063 et 0,9 ± 0,5 ; p < 0,089).
À retenir
Les résultats sont concluants, ils suggèrent que les patients de plus de 60 ans en rémission d’un cancer peuvent pratiquer le yoga en toute sécurité, et que cette pratique permet d’améliorer la fatigue, la qualité de vie globale et sa composante émotionnelle.
• Arana E, Lin PJ, Magnuson A et al. Yoga vs. behavioral placebo for fatigue and quality of life among older cancer survivors. J Clin Oncol 2023 ; 41 : abstr. 12023.
Nicolas Jovenin déclare ne pas avoir de liens d’intérêt en rapport avec cet article.