Les glucocorticoïdes (GC) sont largement utilisés en oncologie pour leur effet immunomodulateur et anti-inflammatoire. Ils peuvent être pourvoyeurs de nombreux effets secondaires, notamment une suppression de l’axe hypothalamo-hypophyso-surrénalien (HHS), et conduire, lors de l’arrêt du traitement, à une insuffisance surrénalienne induite par les glucocorticoïdes (IS-GC) dépendant de la dose, la durée, la puissance du GC, la voie d’administration et la sensibilité individuelle.
L’objectif de cet article est de fournir aux oncologues des conseils pratiques, en s’appuyant sur les recommandations publiées en 2024 conjointement par la Société européenne d’endocrinologie (ESE) et la Société américaine d’endocrinologie (Endocrine Society) (1), pour :
• la diminution (titration) des GC,
• le dépistage et le diagnostic de l’IS-GC,
• la prise en charge de l’insuffisance surrénalienne (substitution, adaptation en cas de “stress”), et l’éducation des patients.
Un traitement prolongé par une dose supra-physiologique de glucocorticoïdes (GC) va systématiquement entraîner une insuffisance corticotrope (suppression de la synthèse d’ACTH par l’hypophyse), responsable d’une insuffisance de sécrétion en cortisol par la glande surrénale (insuffisance surrénalienne induite par les glucocorticoïdes, IS-GC). Elle est le plus souvent réversible, après une durée dépendant de la dose et de la durée de prise de GC. Ce risque existe quelle que soit la voie d’administration des GC. La probabilité et la durée de suppression de l’axe hypothalamo-hypophyso-surrénalien (HHS) dépendent principalement de :
• la dose totale et quotidienne,
• la durée du traitement, la puissance et la demi-vie du GC utilisé,
• la voie d’administration (orale, intra-articulaire, intraveineuse, inhalée, topique – certaines voies systémiques appellent plus de vigilance),
• et la variabilité interindividuelle (sensibilité individuelle, comorbidités, interactions médicamenteuses, notamment les traitements inhibant le CYP3A4).
Qui tester et quand ?
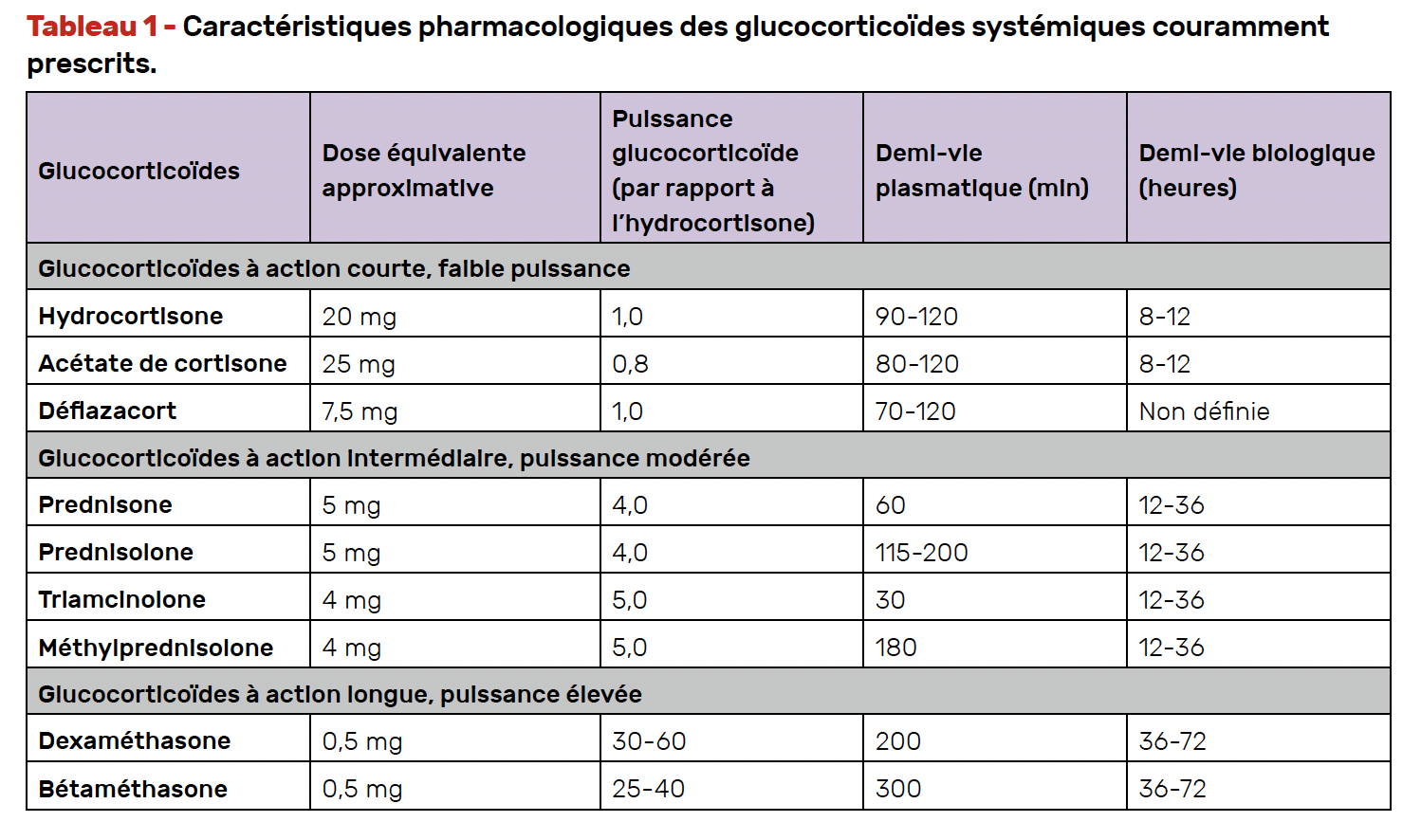
Tout traitement prolongé par GC à doses supra-physiologiques (c’est-à-dire à plus de 15-25 mg/j d’équivalent hydrocortisone ou 4-6 mg/j de prednisone ou prednisolone, 3-5 mg/j de méthylprednisone ou 0,25-0,5mg/j de dexaméthasone (Tab.1)) peut entraîner une IS-GC.
S’il n’y a pas de durée de prise de GC établie en dessous de la laquelle le risque d’IS-GC n’existe pas, ce risque paraît faible en dessous de 3 semaines d’utilisation.
• Pour un traitement de moins de 3 semaines, un arrêt simple sans décroissance et sans test est souvent possible.
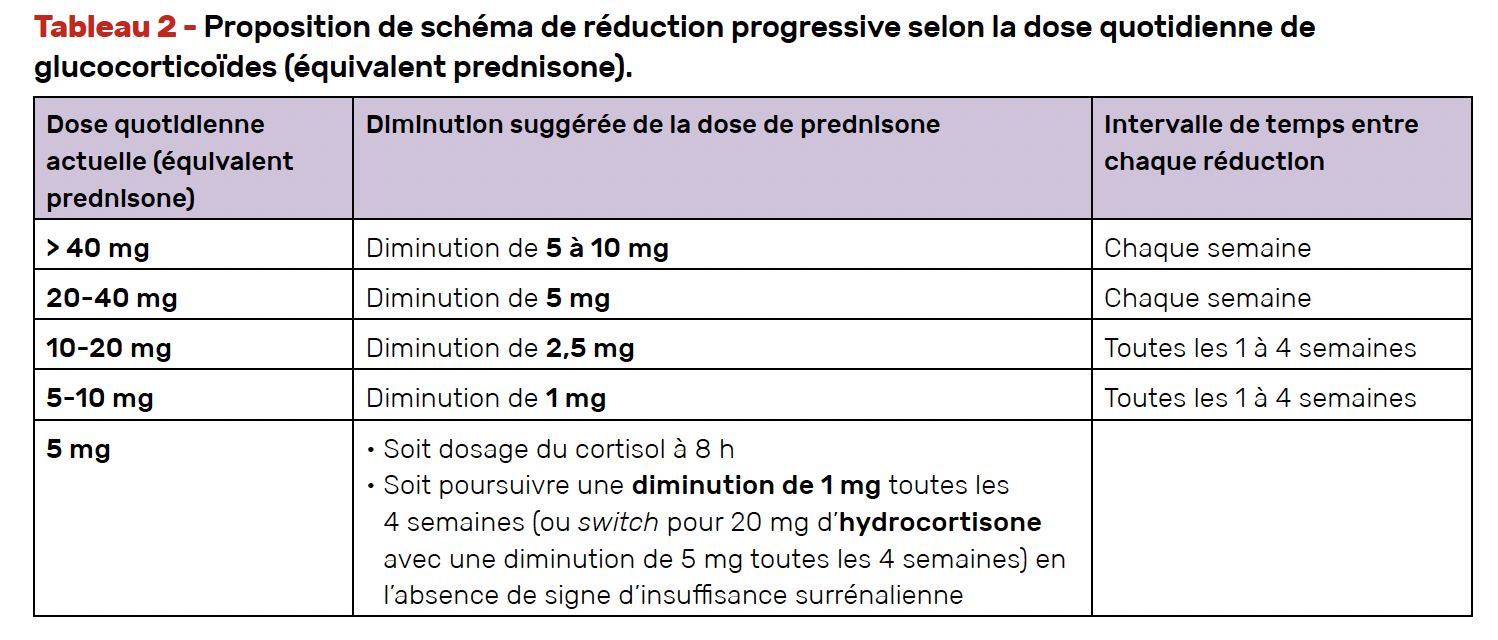
• Pour un traitement de plus de 3 semaines, il faut envisager un sevrage progressif (sur plusieurs semaines ou mois), dont la durée et les modalités dépendent de la dose et de la durée du traitement par GC (un exemple de schéma de décroissance dans le tableau 2).
Le sevrage
• Au cours du sevrage, malgré des doses encore supra-physiologiques, il peut apparaître un syndrome de sevrage en GC (fatigue, myalgies, maux de tête, anorexie…), qui nécessite de revenir à la dernière dose tolérée et ralentir le rythme de diminution.
• Au cours de ce sevrage, un changement vers des formes de GC à courte demi-vie (hydrocortisone ou prednisone) est préférable si cliniquement faisable, pour faciliter l’évaluation de l’axe HHS et le sevrage.
• Lorsque la dose aura été réduite à l’équivalent physiologique (15/25 mg/j d’équivalent d’hydrocortisone en deux ou trois prises (Tab.1)) ou arrêtée, les tests biologiques peuvent être réalisés pour vérifier la récupération de l’axe HHS.
• Certains proposent de continuer la décroissance progressive jusqu’à l’arrêt complet en surveillant cliniquement les signes d’insuffisance surrénalienne (IS) et de ne tester qu’en cas de signe d’IS. Cette conduite à tenir nécessite une bonne éducation thérapeutique du patient et une surveillance clinique régulière du clinicien.
Quels tests ?
Tester la récupération de l’axe HHS ne s’envisage qu’après une décroissance jusqu’à des doses physiologiques de GC (équivalent 15-25 mg/j d’hydrocortisone) et au moins 24 h après la dernière prise de GC (si possible GC à courte demi-vie hydrocortisone ou prednisone).
Le dosage du cortisol
Il est proposé de réaliser un simple dosage du cortisol à 8 h du matin au moins 24 h après la dernière dose de GC, puis, selon le résultat :
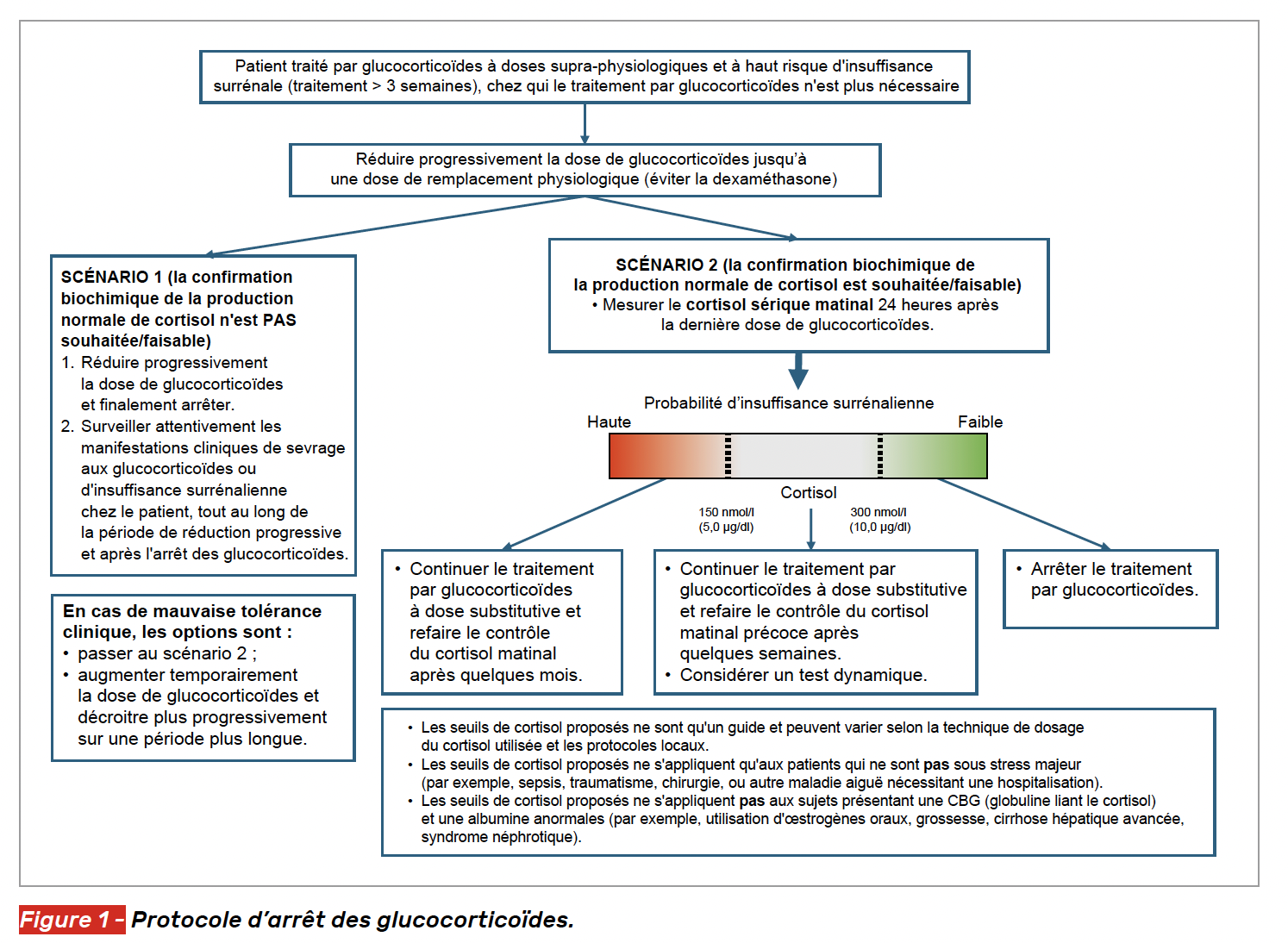
• > 300 nmol/l (~ 10 µg/dl) -> récupération probable : arrêt des GC possible ;
• 150–300 nmol/l (~ 5-10 µg/dl) -> zone indéterminée : continuer la dose physiologique de GC et retester après quelques semaines ou envisager un test dynamique (Synacthène®) ;
• < 150 nmol/l (~ 5 µg/dl) -> insuffisance probable : maintenir la substitution à dose physiologique de GC et réévaluer après quelques mois.
Le test dynamique au Synacthène®
Un test dynamique au Synacthène® (ACTH de synthèse) peut donc être proposé en cas de cortisol matinal intermédiaire pour confirmer une insuffisance. Le test standard repose sur le dosage du cortisol avant, 30 et 60 minutes après injection de 250 µg de Synacthène® IV ou IM. Ce test est considéré comme normal (bonne récupération de l’axe corticotrope) si le cortisol est > 18 µg/dl ou 500 nmol/l.
Cette conduite à tenir est résumée dans la figure 1.
Interprétation des seuils de cortisol
Ces seuils de cortisol ne sont qu’indicatifs et peuvent varier selon la méthode de dosage du cortisol utilisée et les protocoles locaux. Les seuils de cortisol proposés ne s’appliquent qu’aux patients qui ne sont pas en situation de stress (par exemple, sepsis, traumatisme, chirurgie ou autre maladie aiguë nécessitant une admission à l’hôpital). Enfin, ces seuils, reposant sur des dosages de cortisol total, dépendant de la CBG (Cortisol Binding Globulin), ne s’appliquent pas aux sujets présentant un taux de CBG ou d’albumine anormal (par exemple, insuffisance rénale, hépatopathie, syndrome néphrotique…). Il est alors préférable de mesurer le cortisol libre, par exemple salivaire (non remboursé actuellement en France).
Quelle éducation thérapeutique ?
• La prescription d’un traitement prolongé par GC à doses supra-physiologiques expose le patient à un syndrome de Cushing exogène, dont il doit être informé.
• Lors de la décroissance d’un traitement par GC, il faut informer le patient de la possibilité d’un syndrome de sevrage (fatigue, myalgies, maux de tête, anorexie…) et lui donner la possibilité de revenir à la dose antérieurement tolérée et retenter la diminution quelques semaines plus tard.
• Lorsque le traitement se rapproche des doses physiologiques ou en situation de stress peuvent apparaître des signes d’insuffisance surrénalienne (asthénie, nausée, douleur abdominale, vomissement, diarrhée, hyponatrémie, troubles hémodynamiques), qui nécessitent une augmentation du traitement par GC. Il convient d’éduquer le patient à reconnaître ces signes et à savoir augmenter son traitement. Il doit savoir anticiper cette situation et augmenter de lui-même en situation de stress (fièvre, infection, hospitalisation…) pour éviter une crise d’insuffisance surrénalienne aiguë. Cette augmentation de dose peut se faire PO, mais peut nécessiter une injection IV ou SC en cas de persistance de diarrhées ou vomissements malgré l’augmentation des doses PO ou en cas de signes hémodynamiques. Le patient doit être porteur d’une carte d’urgence standardisée.
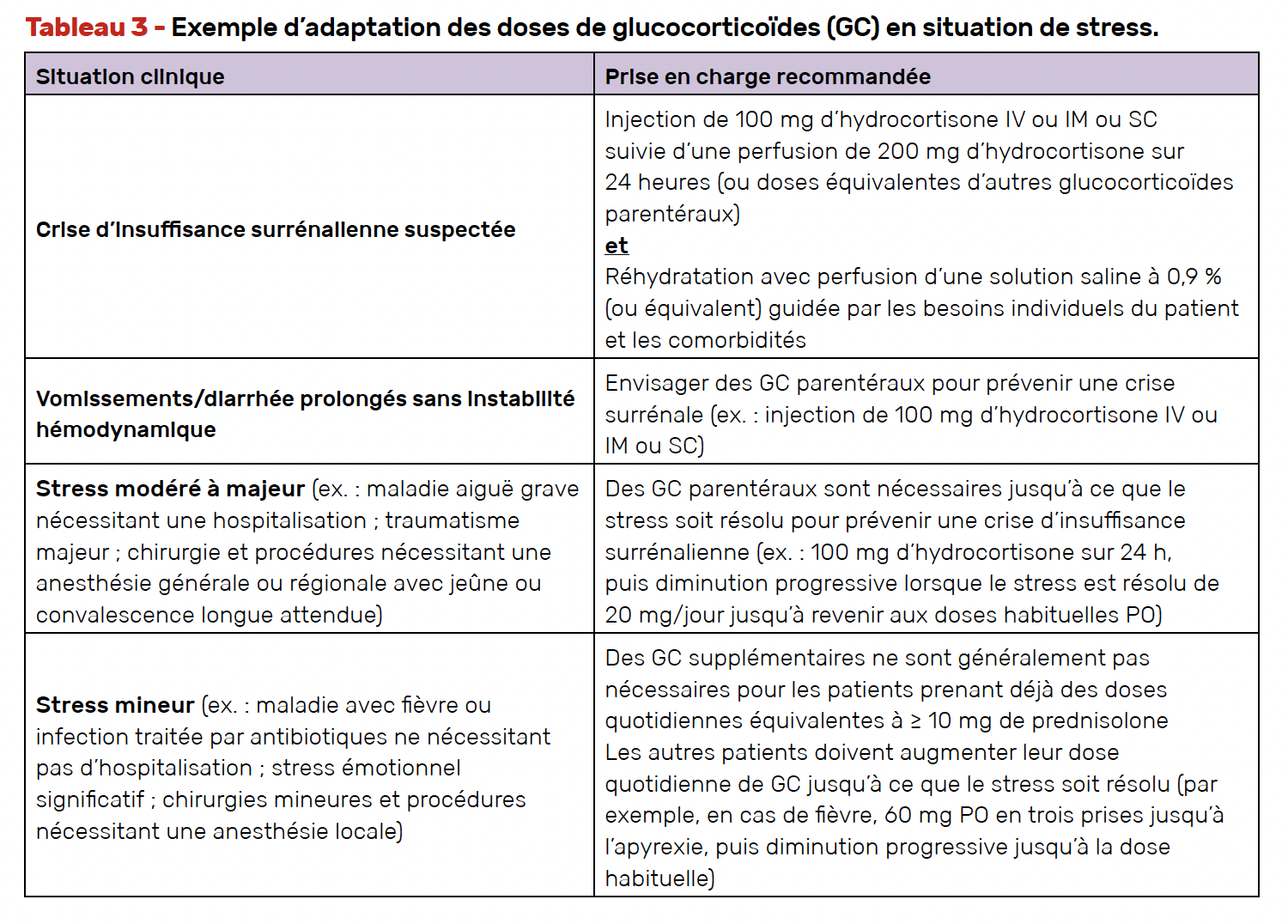
• En cas d’hospitalisation du patient pour un événement aigu ou un geste interventionnel, il convient de lui prescrire de fortes doses d’hydrocortisone (100 à 200 mg/24 h), et de revenir progressivement à sa dose substitutive habituelle sur plusieurs jours.
Des exemples d’adaptations des doses de GC sont proposés dans le tableau 3.
Certains services d’endocrinologie proposent des programmes d’éducation thérapeutique pour la prévention de la décompensation d’insuffisance surrénalienne et l’apprentissage à l’auto-injection d’hydrocortisone en SC.
Quand adresser le patient à un endocrinologue ?
Il est proposé d’adresser le patient à un endocrinologue en l’absence de récupération de l’axe HHS malgré 1 an de traitement à dose physiologique pour éliminer une autre cause d’insuffisance surrénalienne, ou en cas de décompensation surrénalienne (crise d’insuffisance surrénalienne aiguë).
L’auteur déclare ne pas avoir de liens d’intérêt en rapport avec cet article.
Bibliographie
1. Beuschlein F, Else T, Bancos I et al. European Society of Endocrinology and Endocrine Society Joint Clinical Guideline: Diagnosis and therapy of glucocorticoid-induced adrenal insufficiency. Eur J Endocrinol 2024 ; 190 : G25-51.