Onko+ a une nouvelle fois le plaisir de vous faire partager les moments forts des Rencontres scientifiques du GINECO afin de mettre en lumière les dernières avancées dans les cancers gynécologiques et du sein ainsi que les actualités du groupe. Cette année, nous vous proposons un point sur les traitements post-PARP, les nouveaux traitements dans les cancers gynécologiques, les avancées en termes de chirurgie du cancer de l’ovaire, les traitements d’avenir dans les cancers de la vulve, mais aussi la télésurveillance auprès des patientes. Ce dossier est introduit par la présidente du groupe, le Pr Isabelle Ray-Coquard, la vice-présidente, le Dr Anne-Claire Hardy-Bessard, ainsi que par la directrice générale d’ARCAGY-GINECO, Bénédicte Votan, qui dressent le bilan de l’année et les perspectives. Pour finir, Coralie Marjolet retrace les différentes activités de l’association IMAGYN dont elle est présidente.
1/ 18es Rencontres 2024 : c’était une belle édition tant au niveau de la qualité des topos scientifiques que de la super ambiance !
Quels ont été les moments forts de ces rencontres ?
Dr Anne-Claire Hardy-Bessard : Les rencontres en elles-mêmes sont un moment fort de partage scientifique, mais également humain. Leur grand succès montre à quel point elles sont attendues par les onco-gynécologues et les onco-sénologues.
Pr Isabelle Ray-Coquard : Un mélange de science de haut niveau, de retour sur le travail qu’accomplit le GINECO chaque année et de partage de connaissances, mais aussi d’amitié restent les points marquants de la marque de fabrique du GINECO.
Bénédicte Votan : Après l’édition particulière de 2023 pour les 30 ans d’ARCAGY-GINECO, nous avons souhaité revenir à quelque chose de plus classique avec des topos scientifiques et surtout un invité international. Il y a eu beaucoup de moments forts lors de ces 2 jours, mais la présentation du Pr Domenica Lorusso sur l’immunothérapie dans les cancers du col a certainement été l’un des moments forts de ces rencontres.
Quel est le bilan du GINECO pour 2023 ?
Bénédicte Votan : Le bilan est très bon avec 651 inclusions, 16 études ouvertes aux inclusions et 21 publications : une année record en termes de publications !
Pr Isabelle Ray-Coquard : Les chiffres parlent d’eux-mêmes, une reconnaissance nationale européenne et internationale, qui se voit en recherche clinique, mais aussi dans l’investissement du GINECO autour de programmes d’aide à la prise en charge au quotidien que sont le réseau TMRG dédié aux cancers rares, l’association IMAGYN, pour et par les patientes, et, plus récemment, le réseau FEMNET dédié aux cancers féminins de mauvais pronostics.
Dr Anne-Claire Hardy-Bessard : Le GINECO est toujours l’un des groupes européens, voire le groupe européen, qui recrute le plus dans beaucoup d’essais internationaux du GCIG, mais aussi un groupe qui construit des études intéressantes nationales et internationales pour répondre à des questions essentielles.
Quels sont les faits marquants de l’année ?
Bénédicte Votan : Le nombre d’études internationales portées par le groupe n’a jamais été aussi élevé : en effet quatre études internationales sponsor ARCAGY-GINECO (DOMENICA, NIRVANA-1, SENTICOL III et TEDOVA) sont actuellement en cours de recrutement. Ce qui montre bien à quel point le groupe a une dimension internationale incontestée.
Pr Isabelle Ray-Coquard : Ajoutés à ce que Bénédicte a mis en évidence et qui est le cœur de notre activité, la visibilité du GINECO au niveau européen avec la vice-présidence de l’ENGOT, la fin du recrutement de GREAT, qui permettra une belle cohorte de cancers de l’ovaire et le développement du réseau FEMNET autour du groupe GINECO et UCBG.
Dr Anne-Claire Hardy-Bessard : L’année a plutôt été marquée par des actualités dans les cancers du col et de l’endomètre avec des études majeures ayant déjà changé nos pratiques, mais soulevant de nouvelles questions de stratégies thérapeutiques.
Quels sont les prochains enjeux et challenges pour l’avenir ?
Bénédicte Votan : Le challenge pour cette année sera de réussir à maintenir le recrutement dans l’étude DOMENICA, et ce, avant que tous les pays ne puissent avoir accès au dostarlimab. En effet, la question posée par cette étude reste importante et il est vraiment essentiel de pouvoir la terminer rapidement.
Pr Isabelle Ray-Coquard : Un autre défi est celui de la future présidence et vice-présidence du GINECO ouverte à candidature dans le cadre de mandats terminés et non renouvelables. Cette nouvelle gouvernance sera un plus pour le GINECO dans son renouvellement des énergies consacrées au groupe tout en restant en ligne avec les valeurs défendues depuis sa création en 1993.
Dr Anne-Claire Hardy-Bessard : L’avenir proche concerne les résultats de l’étude FIRST qui permettra de trancher sur le rôle ou non de l’immunothérapie dans le cancer de l’ovaire, et aussi l’arrivée des anticorps drogue-conjugués en gynécologie avec de nombreuses phases III en train de s’ouvrir, qui suscitent un grand intérêt et un nouvel espoir pour nos patientes.
Isabelle Ray-Coquard déclare ne pas avoir de liens d’intérêt en rapport avec cet article. Anne-Claire Hardy-Bessard déclare avoir des liens avec AstraZeneca, Clovis, GSK, MSD, Novartis, Pfizer, Roche.
2/ Les leçons de PAOLA-1 : focus sur le post-PARP
D’après la présentation du Pr Isabelle Ray-Coquard (Lyon)
L’essai PAOLA-1 est une étude de phase III, multicentrique, randomisée, en double aveugle, comparant l’olaparib au placebo chez des patientes atteintes de cancer séreux ou endométrioïde de haut grade de l’ovaire, des trompes de Fallope ou du péritoine de stade FIGO IIIB-IV, traitées en première ligne par l’association platine-taxane et bévacizumab. Les résultats de PAOLA-1 ont mis en évidence l’importance des inhibiteurs de PARP (PARPi) en association avec le bévacizumab dans les carcinomes de haut grade de l’ovaire, corroborant les conclusions d’autres études telles que SOLO-1 (olaparib), PRIMA (niraparib) et ATHENA (rucaparib).
Quelles populations ?
Statut HRD
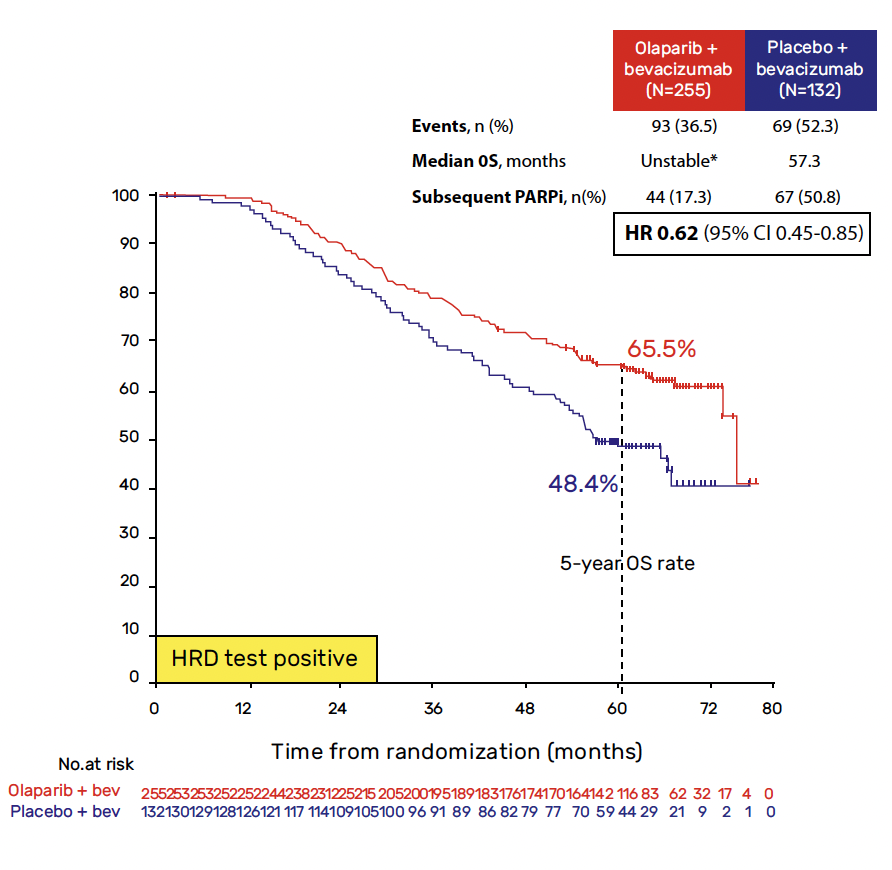
Les patientes HRD+ tirent un bénéfice significatif des PARPi associés au bévacizumab, comme le démontre l’absence de récidive chez environ 50 % des patientes à 5 ans (contre 20 % dans le groupe bévacizumab + placebo). Cela se traduit par une amélioration de la survie globale (SG) avec un taux de survie de 65,5 % à 5 ans dans le groupe olaparib + bévacizumab contre 48,4 % dans le groupe bévacizumab + placebo (Fig. 1). Il s’agit de la seule étude à ce jour montrant un bénéfice en SG dans cette population HRD+ (au-delà de BRCA).
Figure 1 – PAOLA-1 : survie globale à 5 ans des patientes atteintes d’un cancer de l’ovaire de haut grade (sous-groupe HRD-positives) traitées par olaparib + bévacizumab ou placebo + bévacizumab (Ray-Coquard et al. ESMO 2022) .
Âge
L’âge des patientes n’influence pas l’efficacité des PARPi, avec une survie sans progression (SSP) de 21,6 mois dans le groupe âgé (> 65 ans) contre 22,9 mois dans le groupe jeune (< 65 ans). Néanmoins, les profils de toxicité diffèrent : les patientes âgées présentent plus de toxicité hématologique et moins de toxicité digestive que les patientes plus jeunes.
Mutations de BRCA
Des mutations spécifiques de BRCA peuvent moduler l’efficacité des traitements, soulignant l’importance d’une approche individualisée. Par exemple, les altérations du domaine de liaison de RAD51 confèrent une meilleure sensibilité aux PARPi comparées aux altérations du domaine RING.
Statut HRp
Pour la population HRp, des alternatives thérapeutiques sont à l’étude, telles que les anticorps drogue-conjugués (ADC) ciblant Trop2 ou les inhibiteurs de WEE1, notamment pour les tumeurs présentant une amplification de la cycline E1.
Pour quelle durée ?
La gestion de la maintenance en 1re ligne reste débattue, notamment concernant la durée optimale du traitement (2 ans, 3 ans ou jusqu’à progression), ainsi que les aspects liés à la qualité de vie et à la sécurité des patientes. Toutefois, l’avenir semble être à la réduction de la durée de maintenance des PARPi pour permettre leur réintroduction en cas de rechute.
Quel suivi pour détecter une récidive ?
La récidive n’est pas toujours détectée par le CA125, en particulier chez les patientes présentant des mutations BRCA ou HRD+. Cela souligne l’importance d’un suivi rapproché par imagerie, surtout dans les cas de maladie oligométastatique pour lesquels une chirurgie de récidive peut être envisagée.
Quelle thérapeutique après progression ?
L’essai MITO-16 montre qu’il existe un bénéfice à poursuivre le bévacizumab, indépendamment de la progression antérieure sous ce traitement. Concernant l’étude PAOLA-1, l’efficacité de la chimiothérapie à la 1re rechute semble influencée par plusieurs facteurs, tels que l’intervalle libre sous platine, la qualité de la chirurgie initiale et la progression sous traitement par inhibiteur de PARP. Une analyse post-hoc indique que la chimiothérapie à base de platine est moins efficace chez les patientes ayant progressé sous olaparib + bévacizumab comparées à celles n’ayant jamais reçu l’association ou ayant progressé après l’arrêt de l’association (2 ans pour la plupart des patientes du bras olaparib-bévacizumab ; une suvie sans rechute médiane de l’ordre de 7 mois pour les premières versus plus de 12 mois pour les suivantes).
Quid du PARPi post-PARPi ?
Dans l’essai OREO, le rechallenge par olaparib semble prometteur. Chez les patientes en rechute d’un cancer de l’ovaire platine sensible, quel que soit le statut BRCA, cela améliore la SSP (HR = 0,53 (0,38-0,73)). Dans l’analyse post-hoc de PAOLA-1, les patientes qui n’ont jamais reçu de PARPi ou qui ont progressé après l’arrêt du PARPi semblent bénéficier de la même manière d’un entretien par PARPi en 1re rechute contrairement à celles qui ont progressé sous PARPi et un reçu un rechallenge par PARPi à la 1re rechute.
Il pourrait y avoir de bénéfice à rechallenger un PARPi dans les cancers non platine sensibles.
En conclusion
L’essai PAOLA-1 apporte un éclairage intéressant sur la gestion des PARPi dans les différentes populations (BRCA, HRD+, HRD-) et impose de nouveaux questionnements. Les futurs essais devront permettre de déterminer l’intérêt d’un rechallenge par PARPi pour les patientes qui ne progressent pas sous PARPi en 1re ligne et qui sont sensibles à une combinaison à base de platine en 1re rechute et tenter de trouver de nouvelles thérapeutiques pour les populations HRp.
3/ Nouvelles drogues dans les cancers gynécologiques
D’après la présentation du Dr Alexandra Leary (Paris)
Thérapies ciblant l’ADN : focus sur l’inhibition de Wee1
Les inhibiteurs de Wee1 représentent une avancée prometteuse dans le traitement des cancers gynécologiques, particulièrement ceux de l’ovaire et de l’endomètre.
Wee1
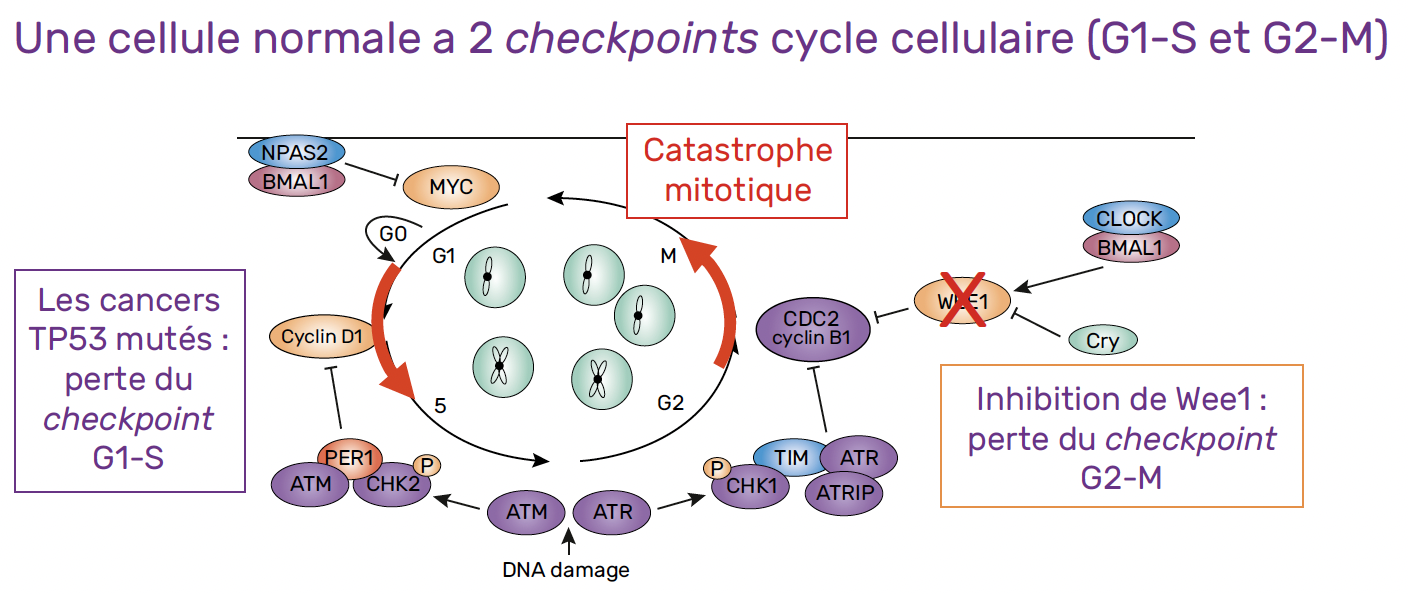
Wee1 est une kinase qui joue un rôle crucial dans la régulation du cycle cellulaire, en particulier lors de la transition de la phase G2 à la phase M. Son inhibition vise à supprimer ce point de contrôle, empêchant ainsi les cellules cancéreuses de réparer leur ADN endommagé avant la division cellulaire, ce qui conduit à leur mort.
Les cancers gynécologiques, en particulier ceux avec des mutations p53, dépendent fortement de ce checkpoint pour leur survie. En ciblant Wee1, les thérapies cherchent à provoquer une catastrophe mitotique, menant à la destruction des cellules cancéreuses (Fig. 1).
Figure 1 – Inhibition de Wee1 : mécanismes d’action.
Résultats
Des études cliniques et précliniques ont montré des résultats prometteurs pour l’inhibition de Wee1 dans ces cancers, notamment avec des taux de réponse significatifs chez les patientes résistantes aux traitements classiques.
• Par exemple, l’azénosertib a démontré un taux de réponse de 37 % en monothérapie.
• De plus, les cancers surexprimant la protéine CCNE1, fréquente dans les cancers séreux de haut grade ou mutés p53, répondent très bien aux inhibiteurs de Wee1, avec un taux de réponse de 57 %.
Ces résultats ouvrent la voie à des essais cliniques plus larges et à une intégration potentielle de ces thérapies dans les pratiques cliniques standard.
La combinaison des inhibiteurs de Wee1 avec d’autres agents ciblant des mécanismes de réparation de l’ADN, comme CHK1, représente une perspective prometteuse pour surmonter la résistance aux traitements et améliorer les résultats pour les patientes atteintes de cancers gynécologiques. Cependant, des défis persistent, notamment en ce qui concerne la sélection des patientes et l’optimisation des combinaisons thérapeutiques.
Les anticorps drogue-conjugués
Principe
Les Antibody-Drug Conjugates (ADC) sont une classe émergente de médicaments qui combinent la spécificité des anticorps avec la puissance des agents cytotoxiques, offrant une nouvelle stratégie pour traiter les cancers gynécologiques.
Les ADC exploitent la capacité des anticorps à cibler spécifiquement des antigènes exprimés à la surface des cellules cancéreuses, permettant ainsi de délivrer une dose élevée de médicament directement aux cellules tumorales.
Résultats
Ces cancers expriment souvent des antigènes spécifiques qui constituent des cibles idéales pour les ADC. Par exemple, les ADC ciblant des antigènes comme CA-125 ou HER2 ont produit des résultats prometteurs.
Des études cliniques ont démontré des taux de réponse significatifs, notamment un taux de réponse de 46 % pour un ADC ciblant CDH6 dans les cancers résistants.
Les ADC représentent donc une nouvelle option thérapeutique pour les patientes qui ne répondent pas aux traitements conventionnels.
Bien que beaucoup d’ADC soient en développement pour les cancers gynécologiques, ces traitements présentent encore des défis, tels que la gestion des effets secondaires et la sélection des patientes les plus susceptibles de bénéficier de cette approche.
Malgré ces obstacles, les ADC constituent une avancée novatrice et prometteuse, ouvrant la voie à des thérapies plus ciblées et potentiellement plus efficaces pour les cancers gynécologiques.
Les immunothérapies de nouvelle génération dans les cancers gynécologiques
Les immunothérapies de nouvelle génération représentent une autre avancée importante dans le traitement des cancers gynécologiques.
Les vaccins
Les vaccins thérapeutiques font partie des approches innovantes.
• Par exemple, un essai associant un vaccin contre les HPV16 et 18 avec pembrolizumab a montré un taux de réponse de 42 % dans les cancers du col métastatiques en rechute post-platine, contre 15 % avec l’immunothérapie seule.
• Par ailleurs, l’essai TEDOVA, utilisant le vaccin Tedopi® (composé d’un cocktail d’antigènes tumoraux comme ACE, HER2, P53, et MAGEA2) a montré des résultats prometteurs en brisant la tolérance immunitaire et en améliorant l’affinité au TCR ou HLA-A2.
Les anticorps bispécifiques
Les bispecific T cell engagers (BiTEs) sont une autre approche notable, utilisant des anticorps bispécifiques pour cibler à la fois les lymphocytes et les cellules tumorales.
Des essais de phase I sont en cours, notamment avec des bispécifiques ciblant CD3 et PRAME ou MUC16 (essai REGENERON).
Les CAR-T cells et les TILs
Déjà connues en hématologie, les CAR-T cells et les lymphocytes infiltrants de tumeurs (TILs) sont des armes thérapeutiques en cours d’évaluation en oncologie solide.
• L’essai SURPASS-3 (en cours), utilisant des lymphocytes modifiés pour cibler MAGE-A4, a montré un taux de réponse de 40 % dans les cancers de l’ovaire résistants, avec des réponses prolongées jusqu’à 12 mois.
• De même, les TILs ont montré un taux de réponse de 45 % chez les patientes avec un cancer du col métastatique post-platine, augmentant à 57 % avec l’ajout de pembrolizumab.
Néanmoins, ces thérapeutiques semblent difficilement transposables à la pratique courante pour le moment en raison d’une toxicité et d’un coût importants.
Malgré ces avancées, les immunothérapies de nouvelle génération font face à des défis tels que la sélection des patients, la résistance acquise et la gestion de la toxicité immunitaire. Néanmoins, elles représentent une voie prometteuse pour améliorer les résultats cliniques et la survie des patientes atteintes de cancers gynécologiques, ouvrant la voie à de nouvelles stratégies thérapeutiques innovantes.
4/ Cancer avancé de l’ovaire : les nouveautés en chirurgie
D’après la présentation du Pr Jean-Marc Classe (Nantes)
Malgré les avancées thérapeutiques récentes, le cancer de l’ovaire demeure une pathologie complexe où la chirurgie conserve une place centrale dans la prise en charge. Les études prouvent qu’une chirurgie complète est associée à une meilleure survie, montrant ainsi l’importance de qualité de la chirurgie et la nécessité de l’optimiser.
Place des curages ganglionnaires
• L’essai LION avait pour objectif d’étudier l’utilité des curages ganglionnaires dans la prise en charge des cancers ovariens. Les résultats indiquent qu’en cas d’évaluation scanner ou clinique per-opératoire ne révélant pas de ganglions suspects en situation de chirurgie première, il n’y a pas d’intérêt à réaliser un curage.
• Dans le contexte de la chirurgie d’intervalle, les résultats de l’essai CARACO sont concordants avec les résultats de LION : il n’y a pas de bénéfice à effectuer systématiquement un curage pour les patientes sans ganglion suspect détecté avant l’intervention.
Cependant, pour les patientes présentant des ganglions suspects avant l’intervention, le curage reste une étape importante dans le processus de stadification de la maladie.
Nombre optimal de cures de chimiothérapie
Le nombre optimal de cures de chimiothérapie néoadjuvante est un sujet de débat. Les recommandations préconisent trois ou quatre cures, mais il existe des variations en fonction des pratiques cliniques (jusqu’à six cures).
L’essai CHRONO vise à clore le débat en comparant ces deux modalités (six cures de chimiothérapie par rapport à trois), afin d’évaluer leur effet sur la survie et la réponse tumorale.
Nouveaux outils pour moduler le timing de l’indication chirurgicale
De nouveaux outils sont en développement pour optimiser le timing de l’indication chirurgicale dans le traitement des cancers de l’ovaire. La notion de chimio-sensibilité est de plus en plus prise en compte, avec des critères pathologiques, génomiques et biologiques émergents. Par exemple, des signatures génomiques commencent à être utilisées pour prédire la réponse tumorale à la chimiothérapie. De plus, certains critères biologiques, comme le score de KELIM, sont également étudiés pour guider la décision clinique.
Chimiothérapie hyperthermique intra-péritonéale (CHIP)
La CHIP est une option thérapeutique pouvant être utilisée dans la prise en charge des cancers de l’ovaire, principalement dans les situations avancées ou en cas de récidive.
L’essai OVHIPEC 1
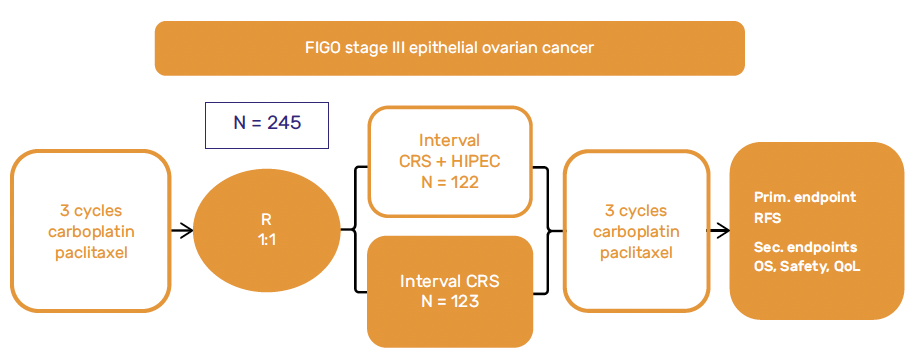
Plusieurs essais cliniques, dont l’essai OVHIPEC 1, ont montré des résultats prometteurs pour la CHIP. Dans cet essai, les patientes non opérables d’emblée ont reçu trois cures de carboplatine-paclitaxel, suivies d’une chirurgie d’intervalle avec ou sans CHIP, puis trois autres cures de carboplatine-paclitaxel (Fig. 1).
Figure 1 – OVHIPEC 1 : design de l’essai.
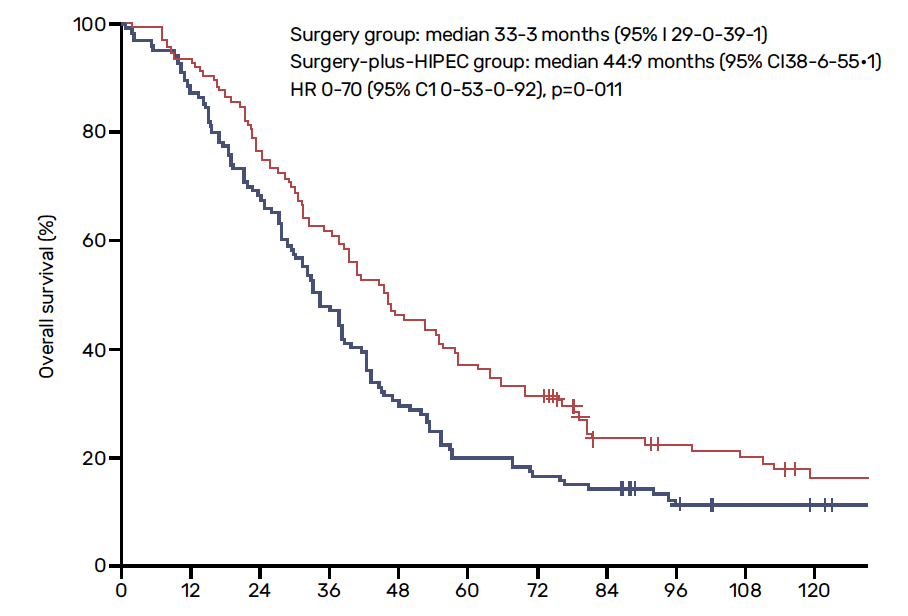
Les résultats à long terme de cet essai ont montré une amélioration significative de la survie pour les patientes ayant reçu la CHIP. À 10 ans, il persiste un avantage pour le groupe ayant reçu la CHIP, avec une médiane de survie de 44,9 mois comparée à 33,3 mois pour le groupe sans CHIP (HR = 0,7 ; IC 95 % = 0,53-0,92) (Fig. 2). De plus, la qualité de vie des patientes n’a pas été significativement altérée par les effets secondaires initiaux de la CHIP.
Figure 2 – OVHIPEC 1 : survie globale (médiane) à 10 ans (Aronson et al. Lancet Oncol 2023).
L’essai CHIPOR
Dans le cas des récidives de cancer de l’ovaire, l’essai CHIPOR a également confirmé les bénéfices de la CHIP. Étaient sélectionnées les patientes avec une récidive au moins 6 mois après la fin du traitement. Elles étaient traitées par chimiothérapie pré-opératoire (jusqu’à six cycles) avant d’être opérées. Pendant l’intervention, si la chirurgie était complète, les patientes étaient randomisées pour recevoir soit la CHIP, soit aucun traitement supplémentaire. Cette population était caractérisée par un taux élevé de séreux de haut grade (80 %) et une forte proportion de chirurgies complètes (87 %).
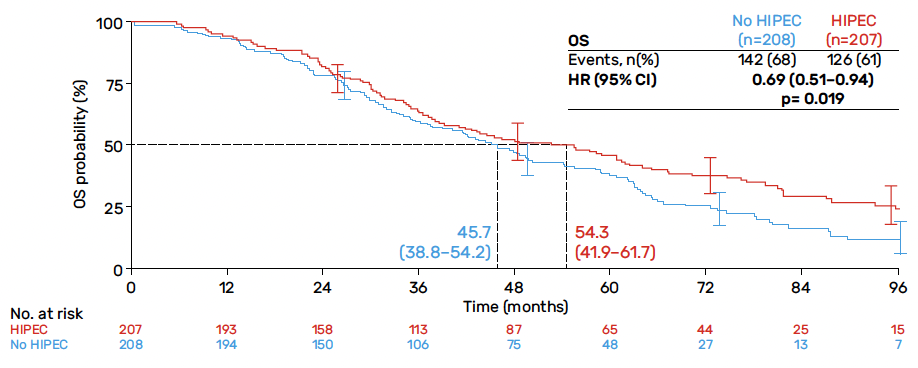
Les patientes ayant bénéficié de la CHIP ont présenté une survie significativement prolongée par rapport à celles n’ayant pas reçu la CHIP (médiane de survie de 45,7 versus 54,3 mois en faveur de la CHIP ; HR = 0,69 ; IC 95% = 0,51-0,94 ; p = 0,02) (Fig. 3), avec des taux de complications globalement similaires entre les deux groupes après l’utilisation du thiosulfate.
Figure 3 – CHIPOR : survie globale (Classe et al. ASCO 2023).
Ces résultats soulignent la pertinence de la CHIP comme modalité thérapeutique dans le traitement des cancers de l’ovaire avancés et récidivants, bien que des questions subsistent sur son application optimale et ses critères de sélection.
Conclusion
La chirurgie reste incontestablement au cœur de la prise en charge du cancer de l’ovaire. Malgré l’introduction des thérapies ciblées telles que les PARPi, l’obtention d’une chirurgie complète demeure un facteur pronostic essentiel.
Avec l’émergence de nouvelles modalités thérapeutiques comme la CHIP, les perspectives dans le traitement des formes avancées et récidivantes du cancer de l’ovaire évoluent. Cette évolution souligne la nécessité d’une adaptation constante de la pratique chirurgicale pour tirer parti des avancées thérapeutiques.
5/ Cancers de la vulve : les traitements d’avenir
D’après la présentation du Dr Frédéric Selle (Paris) et du Dr Gwenaël Ferron (Toulouse)
Le cancer de la vulve représente environ 5 % des cancers gynécologiques, dont 90 % sont des carcinomes épidermoïdes de la vulve (CEV). Le diagnostic se fait le plus souvent autour de l’âge de 70 ans. L’incidence augmente progressivement en Europe, à raison de trois à cinq nouveaux cas pour 100 000 habitants par an. Une tendance notable est la diminution de l’âge de survenue, notamment en lien avec l’infection par HPV. 40 % des CEV sont associés à HPV (HPV16 en représente 75 %) d’où l’importance de la vaccination (y compris retardée). La survie dépend principalement du stade initial de la maladie, avec des taux de survie significativement meilleurs chez les patientes sans atteinte ganglionnaire (75 % de SSP à 3 ans et 90 % de SG) par rapport à celles avec atteinte ganglionnaire (35,2 % de SSP à 3 ans et 56,4 % de SG).
Classification histo-moléculaire
Les cancers de la vulve se classent en fonction de leur statut HPV :
• les carcinomes HPV-dépendants, pour lesquels on retrouve une inactivation de P53 et Rb par les oncoprotéines E3 et E4, conduisant à une expression de P16 (100 % de sensibilité et 98 % de spécificité dans la détection des CEV associés à HPV) ;
• les cancers HPV-indépendants, qui sont souvent liés à des conditions préexistantes comme le lichen scléreux ou des néoplasies intra-épithéliales vulvaires (VIN).
Plus récemment, une distinction en fonction des sous-types moléculaires a été faite, distinguant les cancers HPV-associés P16 positifs avec P53 wild type (meilleur pronostic) ou muté et les cancers HPV-indépendants P53 wild type ou muté (mauvais pronostic).
Traitement en fonction des stades
Stade local
Traitement loco-régional et reconstruction
Le traitement des stades précoces (I et II) implique la résection chirurgicale de la tumeur avec des marges adéquates (> 8 mm en chirurgie, 3 mm en anatomopathologie). Il est crucial de minimiser les chirurgies mutilantes en tenant compte des structures médianes comme l’urètre, le clitoris et l’anus.
La reconstruction est essentielle pour améliorer la qualité de vie, éviter les cicatrices rétractiles, et permettre une reprise de la sexualité. Les techniques modernes de reconstruction utilisent des lambeaux perforants, qui réduisent les complications en prélevant uniquement la peau nécessaire.
Stadification ganglionnaire et essai GROINSS-V
L’essai GROINSS-V a joué un rôle crucial dans l’évolution de la méthode de stadification ganglionnaire pour le cancer de la vulve. Voici un détail des différentes étapes de cet essai :
• GROINSS-V I – Cette première phase a évalué la faisabilité et la sécurité de l’utilisation du ganglion sentinelle chez les patientes avec des tumeurs N0 cliniques et échographiques. La technique combinait une double détection par isotope et bleu de méthylène. Les résultats ont montré un excellent taux de survie à 10 ans et un faible taux de récidive locale (2,5 %) chez les patientes avec un ganglion sentinelle négatif.
Ainsi, le ganglion sentinelle s’est avéré être une méthode sûre et moins morbide par rapport au curage ganglionnaire complet.
• GROINSS-V II – Cette phase s’est concentrée sur les patientes avec des ganglions sentinelles positifs. Elle a examiné si une radiothérapie inguinale (50 Gy) pouvait remplacer la chirurgie de ré-opération ganglionnaire (curage complet) chez ces patientes. À noter que l’étude a fait l’objet d’un amendement afin de réaliser une radiothérapie exclusive en cas de micrométastase (< 2 mm) et un curage ganglionnaire + radiothérapie en cas de macrométastase (> 2 mm).
Les résultats ont montré que l’association ganglion sentinelle positif et radiothérapie réduisait significativement la morbidité par rapport au curage ganglionnaire complet, tout en maintenant un faible taux de récidive locale (1,6 % à 2 ans en cas de micrométastase).
• GROINSS-V III – Cet essai (qui n’a pas encore débuté) explore l’utilisation de la radio-chimiothérapie (56 Gy, avec cisplatine hebdomadaire) pour les patientes avec des macrométastases > 2 mm. L’objectif est de déterminer si la radio-chimiothérapie peut éviter le besoin d’un curage ganglionnaire additionnel, en améliorant les résultats tout en réduisant les complications associées aux interventions chirurgicales.
Stade III non résécable
Pour les stades localement avancés, le traitement standard comprend une approche multidisciplinaire : la combinaison de cisplatine hebdomadaire à 40 mg/m² sur une période de moins de 50 jours est la référence, avec une évaluation de la réponse à 12 semaines.
Les taux de réponse clinique complète sont significatifs (64 %), et les réponses histologiques complètes atteignent 50 %. Chez les patientes ayant reçu une radio-chimiothérapie, la nécessité d’une chirurgie supplémentaire est débattue.
Perspectives
Il s’agit d’optimiser l’approche médicale pour les tumeurs inopérables grâce à l’utilisation de biomarqueurs. Les cancers HPV16-dépendants montrent des taux de réponse complète plus élevés que les P16-négatifs. L’imagerie, notamment le TEP post-traitement, aide à prédire les résultats et la survie après la radiothérapie curative. Des stratégies de radiothérapie exclusive peuvent être envisagées pour les cancers vulvaires HPV-associés, en réduisant les doses pour diminuer la morbidité des exentérations.
26 % des tumeurs vulvaires étant en dMMR, il existe également un rationnel à l’utilisation de l’immunothérapie en néoadjuvant.
Cancer vulvaire métastatique
Pour les cancers vulvaires métastatiques, plusieurs options thérapeutiques sont disponibles.
La chimiothérapie
Les combinaisons de cisplatine-taxol ou carboplatine-taxol sont la référence en traitement de première ligne.
Les thérapies ciblées
• Bévacizumab : par analogie au cancer du col métastatique, peut être utilisé en combinaison avec la chimiothérapie pour certaines patientes.
• Anti-EGFR : environ 11 % des cancers HPV-indépendants montrent une amplification d’EGFR.
• Immunothérapie : pembrolizumab, nivolumab et cimiplimab. Par exemple, Keynote 158 (étude de phase II) a montré un taux de réponse objective de 10,9 %, indépendamment de l’expression du PD-L1.
Conclusion
Le cancer de la vulve est souvent considéré comme le “cancer oublié” de la femme, en raison de sa rareté et de la complexité de sa prise en charge. La recherche clinique est difficile, principalement en raison de l’âge avancé et des comorbidités des patientes. Cependant, une meilleure compréhension de la biologie moléculaire de ces tumeurs et des approches thérapeutiques ciblées pourrait améliorer les résultats cliniques.
Il est essentiel de favoriser la prise en charge dans des centres spécialisés et de promouvoir la recherche clinique pour optimiser le traitement des patientes atteintes de ce type de cancer.
6/ Patientes connectées en gynécologie : télésurveillance, on s’y met ?
D’après la présentation du Pr Florence Joly (Caen) et du Dr Jérôme Martin-Babau (Plérin)
Le développement de la télésurveillance dans le traitement des cancers gynécologiques et du sein est un virage majeur dans la prise en charge des patientes. Cette pratique permet de suivre à distance les données médicales des patientes, ce qui peut conduire à une meilleure adaptation des traitements et à une prise en charge plus efficace certifiée en cas de besoin.
Suivi des symptômes et toxicités
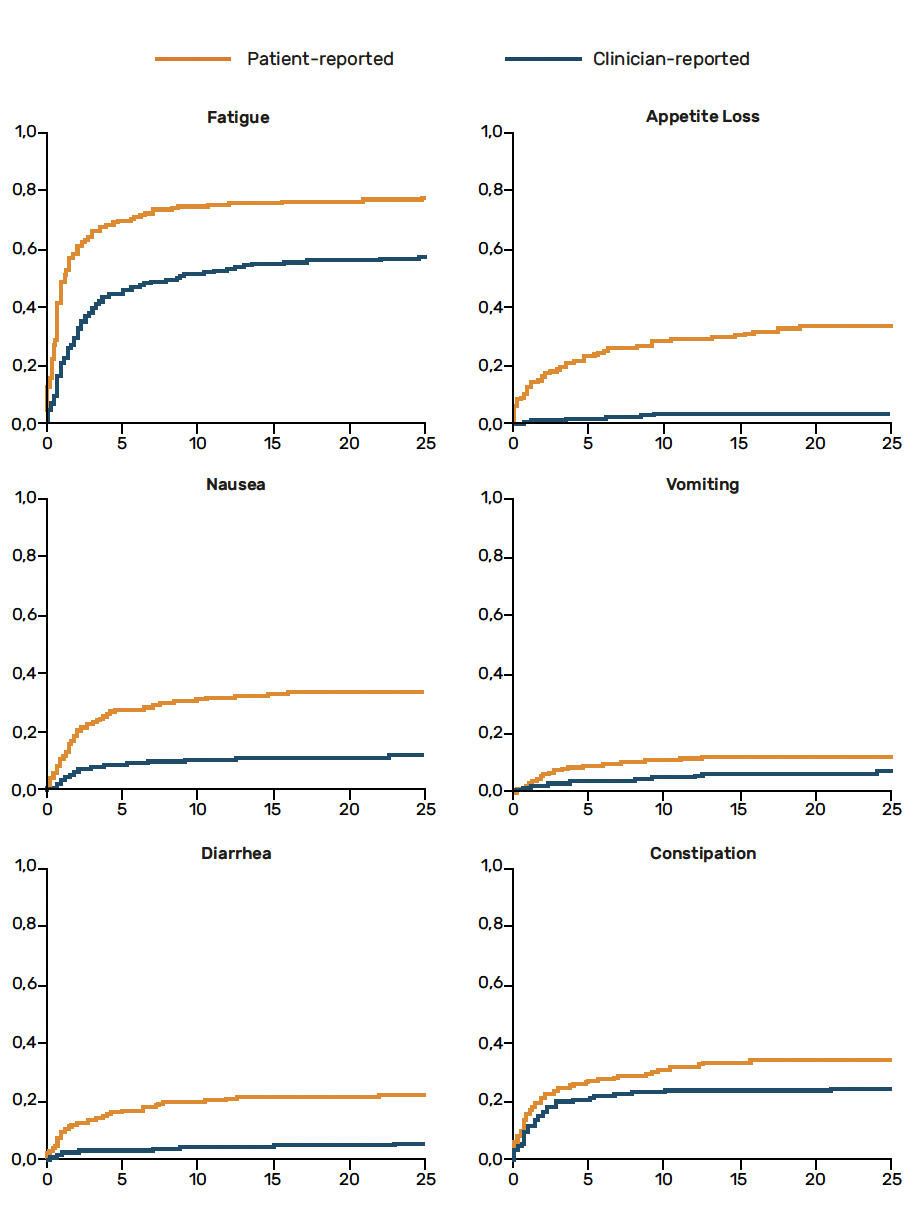
Les patientes sont les mieux placées pour rapporter leurs symptômes et leurs toxicités (Fig. 1), symptômes qu’elles ont parfois du mal à verbaliser lors des consultations médicales traditionnelles. Et les médecins identifient mal ces symptômes. La télésurveillance médicale permet de pallier ce problème en recueillant des données sur l’état de santé des patientes depuis leur lieu de vie (structure médico-sociale ou domicile).
Figure 1 – Incidence cumulée du reporting des symptômes entre cliniciens et patients au fil des semaines (Basch et al. N Engl J Med 2010).
Reconnaissance et intégration de la télésurveillance
Depuis juillet 2023, la télésurveillance en oncologie est reconnue comme un acte médical valorisé. Cela implique l’utilisation de dispositifs médicaux numériques certifiés, la signature de conventions entre les établissements de santé et les fournisseurs de ces dispositifs et la prescription par les médecins de dispositifs médicaux numériques (DMN).
Mise en pratique
En pratique, les patientes remplissent des informations sur leur état de santé via une application sur leur téléphone, et les professionnels de santé reçoivent des alertes en cas de besoin d’intervention. Cette approche est jugée utile pour le suvi de toutes les patientes (avec des niveaux de preuve plus importants pour les stades métastatiques que pour les stades précoces), pendant et après les traitements.
À l’heure actuelle, ce genre de dispositif est uniquement remboursé pour les patientes en cours de traitement.
Études d’efficacité
Des études ont évalué l’efficacité de la télésurveillance en oncologie.
• Par exemple, une étude menée par Basch et al. a montré que les patients télésuivis avaient une moindre dégradation de la qualité de vie (baisse de 1,4 versus 7 points sur l’échelle EQ5D, p < 0,001), moins d’admissions aux urgences (34 versus 41 %, p = 0,02), et une durée plus longue de chimiothérapie (8 versus 6 mois, p = 0,002). Étonnamment, les patients sans expérience informatique en ont tiré un bénéfice encore plus net. Cette étude reposait sur l’auto-évaluation de 12 symptômes avant et entre les visites, avec des rappels hebdomadaires par e-mail pour les patients et les infirmières. Un rapport était préparé pour l’oncologue lors de la consultation, comparé au suivi habituel.
• De même, l’étude CAPRI, un essai de phase III monocentrique à l’IGR, a évalué l’effet du télésuivi supervisé par une infirmière pour les thérapies anticancéreuses orales chez des patients métastatiques. Les résultats ont montré une meilleure adhérence au traitement et une réduction des toxicités chez les patients télésuivis.
Effet sur la survie et la gestion des symptômes
Il n’y a pas, actuellement, assez de données pour conclure sur l’effet de la télésurveillance sur la survie des patientes atteintes de cancer gynécologique.
Perspectives
L’avenir repose sur l’intégration de la télésurveillance en routine pendant les traitements mais également sur la période du suivi post-cancer, bien que cela nécessite davantage d’études pour évaluer son efficacité dans cette phase de la prise en charge des patientes. Plusieurs essais ont été développés en ce sens au sein du groupe GINECO (NiQole dans le cancer de l’ovaire pour le suivi du niraparib, Aftergyn dans l’après-cancer du cancer de l’ovaire et de l’endomètre, Perspective dans le suivi des traitements pour un cancer du sein triple négatif métastatique).
Conclusion
La télésurveillance offre la possibilité d’un suivi plus étroit et personnalisé des patientes, avec des bénéfices potentiels en termes de qualité de vie et de gestion des symptômes. Cependant, son intégration dans la pratique clinique en oncologie gynécologique est encore balbutiante et nécessite des études supplémentaires pour évaluer sa faisabilité et son bénéfice réel et une organisation adaptée est nécessaire pour en maximiser les bénéfices.
7/ Les actions d’IMAGYN en 2022-2023
Quels ont été les événements marquants au niveau institutionnel pour cette année 2023 ?
Coralie Marjollet : Cette année 2023 a été, pour IMAGYN, une année de reconnaissance institutionnelle sur tous les plans : tout d’abord avec le renouvellement de l’agrément national pour 5 ans paru au Journal officiel du 28 novembre dernier couplé à une invitation à intervenir comme exemple de l’effet des actions d’une association agréée sur les politiques de santé lors de la journée des associations agréées au ministère de la Santé le 14 novembre 2023 ; puis avec sa participation à de nombreuses consultations HAS pour l’accès à des thérapies innovantes ou l’obtention du remboursement de nouvelles thérapeutiques ou encore en continuant à participer à la commission d’évaluation du cannabis thérapeutique à l’ANSM. IMAGYN a également été auditionnée par le Haut Conseil à la vie associative et participe activement au groupe de travail mis en place par la mairie de Paris dans le cadre de la refonte de sa stratégie cancer.
En parallèle, l’activité d’IMAGYN, au sein du collectif Demain sans HPV, ne faiblit pas avec un grand nombre d’actions d’information et de sensibilisation à la vaccination contre les papillomavirus humains (HPV) pour accompagner la vaccination dans les collèges pour les élèves de 5e avec la création d’un flyer Parents/Jeunes, la réalisation d’une belle campagne sur Doctolib durant la semaine de la vaccination en avril 2023, une intervention sur la grande scène des Solidays en juin ou encore l’intervention dans différentes réunions et congrès (EUROGIN, colloque « Accélérer la prévention sur les cancers HPV induits », journée Prévention à l’Assemblée nationale).
Et pour les missions de partage et de soutien des patientes et des proches ?
Le COCON (projet réalisé en partenariat avec GSK) s’est installé pendant 2 jours dans cinq villes pour sa tournée 2023 pour aller au plus près des patientes et des proches et les accompagner pendant la maladie.
Nous avons également complété la collection de nos livrets pédagogiques par une édition sur « les bienfaits de l’activité physique » réalisée avec la participation de médecins du GINECO qui ont aussi continué à être très actifs dans l’organisation de webinaires à destination des patientes soutenus par la SFCO, avec, entre autres, un webinaire dédié au cancer de l’endomètre pendant juin vert (mois de sensibilisation aux cancers de l’endomètre et du col de l’utérus), ou le traditionnel webinaire HPV pour répondre à toutes les questions sur ce virus méconnu et sa prévention par la vaccination et le dépistage.
De plus, en parallèle des Cafés IMAGYN en présentiel et en distanciel, des Cafés Jeunes, destinés au moins de 40 ans, ont été mis en place afin d’accompagner plus spécifiquement cette tranche d’âge pour laquelle les conséquences de la maladie et des traitements diffèrent des Cafés IMAGYN traditionnels.
Et bien sûr, l’organisation de septembre turquoise, avec plus de 50 manifestations partout en France au plus près des patientes dans tous les types de centres, privés, publics et anticancéreux, a été un moment fort dans l’accompagnement dans la maladie.
Quelles sont les actions en cours et futures pour faire reculer l’inégalité d’accès aux soins dans les cancers gynécologiques ?
IMAGYN reste très investie dans l’application du décret d’avril 2022 pour la mise en place des critères de qualité d’accès aux soins dans le cancer de l’ovaire et la participation aux réunions en région organisées par le réseau FEM-NET. IMAGYN a aussi participé le 25 avril 2023 à un webinaire avec l’INCa, UNICANCER et la SFCO sur le sujet et, face à l’inaction des autorités pour mettre en place ce décret, continue à agir avec notamment un nouveau webinaire pour faire un état de la situation le 13 mai 2024, une alerte de la presse et des parlementaires face à cette situation délétère pour les patientes qui sont confrontées à une vraie perte de chance quand elles sont prises en charge dans des centres qui ne respectent pas les critères définis par l’INCa.
Quelles sont les autres actions prévues pour cette année 2024 ?
Le COCON, qui maintenant s’appelle “le COCON et son village”, car des tentes sont prévues pour pouvoir développer les activités pour les patientes et les proches, va repartir dans quatre villes. Le programme des webinaires construits pour et avec les patientes est finalisé, un livret sur la douleur va être publié pour le démarrage de septembre turquoise, qui s’annonce déjà comme un mois majeur de sensibilisation et d’information du grand public avec un certain nombre d’actions phares.
Comme chaque année, nous vous invitons à suivre toute notre actualité sur le site de l’association www.imagyn.org, qui va aussi être entièrement refondu pendant l’été, et par le biais de nos réseaux sociaux : Instagram, Facebook, LinkedIn et Twitter.
IMAGYN tient à remercier tous ses soutiens, médecins, professionnels de santé, soutiens financiers et bien sûr ses bénévoles qui, au quotidien, agissent sur le terrain pour accompagner les malades et améliorer l’information sur ces maladies encore méconnues.